Trop-2伴随诊断,你准备好了吗?
020年,FDA批准全球首款靶向TROP2 ADC药物IMMU-132(Sacituzumab Govitecan,戈沙妥组单抗)以来,国内已申报了多款Trop2 ADC新药,其中6月7号云顶新耀引进的Trodelvy已在中国获批上市,国内首款自主研发的Trop2 ADC(科伦药业,SKB264)也已进入3期临床阶段,Trop-2靶点的药物管线也愈加受到重视。本文对Trop 2靶点的相关知识及其检
2020年,FDA批准全球首款靶向TROP2 ADC药物IMMU-132(Sacituzumab Govitecan,戈沙妥组单抗)以来,国内已申报了多款Trop2 ADC新药,其中6月7号云顶新耀引进的Trodelvy已在中国获批上市,国内首款自主研发的Trop2 ADC(科伦药业,SKB264)也已进入3期临床阶段,Trop-2靶点的药物管线也愈加受到重视。本文对Trop 2靶点的相关知识及其检测方法进行整理总结,希望能给予大家一些帮助,也欢迎大家后台积极留言,与我们讨论。
Trop-2简介
早在1981年,人们通过单克隆抗体技术,在人体滋养层细胞表面发现了一种抗原[1],这个抗原被称之为人滋养细胞表面糖蛋白抗原2 (Trop-2)。Trop-2是由染色体1p32区域TACSTD2基因编码表达的细胞表面糖蛋白,属于跨膜蛋白。
Trop-2蛋白结构主要分为胞外区、跨膜区和胞内区三个部分。胞外区又包含3个结构域:1个富含半胱氨酸的结构域,1个甲状腺球蛋白1型结构域和1个缺乏半胱氨酸的结构域 [2](图1)。
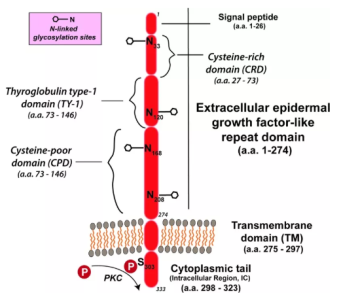
图1.Trop-2蛋白结构组成
Trop-2作用机制
Trop-2是调节细胞周期的细胞膜蛋白,与细胞增殖、分化相关。它的作用机制包括:①增加Ki-67的表达;②促进细胞周期蛋白D、E的表达;③调动细胞内储存的Ca2+,促进细胞增殖;④直接激活MAPK信号通路,激活下游的AP-1,促进细胞分化与增殖[2](图2)。
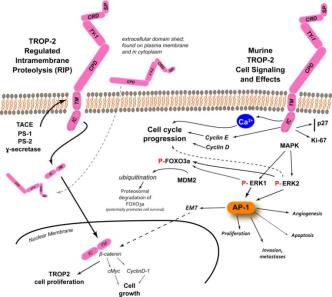
图2.Trop-2的作用机制
Trop-2过表达不仅能够通过JAK/STAT、Bax、Bcl-2、ERK、Akt等通路促进肿瘤细胞增殖、分化和转移,而且能够使PARP1表达增加,导致DNA复制增加和损伤累积,此外,TROP-2的胞内结构域(ICD)的激活还可以促进肿瘤细胞增殖,诱导上皮间充质转化(EMT),促进肿瘤细胞迁移、侵袭和抗凋亡,最终导致肿瘤进展[3](图3)。
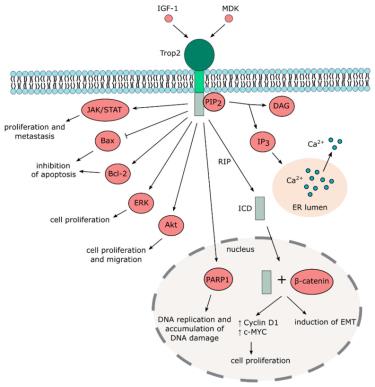
图3.Trop-2在肿瘤中的作用机制
Trop-2的表达
Trop-2是一种主要表达于上皮细胞的跨膜糖蛋白,在人体多种健康组织中有着不同水平的表达,包括前列腺腺体、宫颈复层鳞状上皮细胞、肺泡细胞、乳腺腺体、子宫内膜(图4A);另外在肾集合管、胸腺小体(Hassall's corpuscle)、皮肤、胰腺和肝脏中也有少量表达[4](图4B)。
据文献报道,Trop-2在卵巢癌、结肠癌和甲状腺癌中过度表达,而在相应正常组织中几乎没有表达(图5)。此外,在乳腺癌、宫颈癌、食道癌、肺癌、胰腺癌、前列腺癌、胃癌、膀胱癌和子宫内膜癌上也可见Trop-2表达[4](图4)。
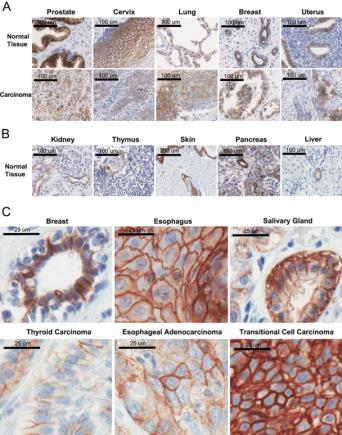
图4.人类Trop-2蛋白表达(一)
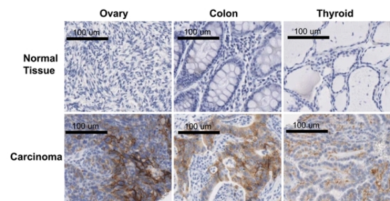
图5. 人类Trop-2蛋白表达(二)
如前文所述,虽然在多种人体正常组织中有Trop-2的表达,但其表达量很低,而在多种肿瘤组织中Trop-2表达明显升高[4]。在乳腺癌尤其是三阴性乳腺癌、宫颈癌、尿路上皮癌、甲状腺乳头状癌中的Trop-2表达最为常见,表达率在80~90%;同时,在肺癌、子宫内膜癌、前列腺癌、胰腺癌、结直肠癌等肿瘤中,Trop-2也存在较高的表达[5-7]。




乳腺癌 结肠癌 胃癌 肺癌
Trop-2恶性肿瘤染色示意图(来自熙宁生物IHC实验室)
检测Trop-2表达水平的意义
一项Meta分析纳入16项研究共2596例实体瘤患者,研究Trop-2过表达与疾病预后的关系。结果显示:Trop-2过表达与更差的总生存期(OS)、无病生存期(DFS)显著相关[8]。另外一项研究也总结了Trop-2过表达与部分肿瘤的不良预后相关[9],详见表1。
表1.Trop-2的过表达与实体瘤患者的不良预后显著相关
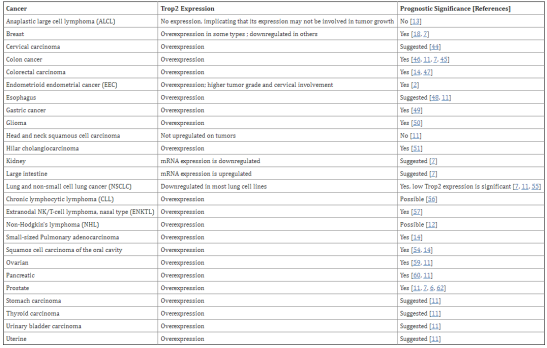
Trop-2在肿瘤细胞中表达显著高于正常细胞,且Trop-2的过表达与实体瘤患者的不良预后显著相关,因此抑制Trop-2后,肿瘤细胞增殖能力减弱[11],是肿瘤治疗的理想靶点。Trop-2 ADC药物正是通过靶向识别Trop-2过表达的肿瘤细胞来达到杀伤肿瘤细胞的目的,检测Trop-2蛋白的表达水平,对临床试验入组及伴随诊断开发具有重要意义。
2020年4月22日,美国FDA已加速批准Immunomedics公司的ADC药物IMMU-132上市,用于治疗经治转移性三阴性乳腺癌(mTNBC)患者。这让戈沙妥珠单抗(Sacituzumab govitecan)成为首款获得FDA批准治疗mTNBC患者的靶向Trop-2的ADC(antibody-drug conjugate,抗体药物偶联物)药物。这也是全球首款获得监管机构批准的靶向Trop-2的ADC药物。2022年6月10日被相关公司引进国内。
在戈沙妥珠单抗的Ⅲ期临床ASCENT研究(NCT02574455)中,虽然不同Trop-2表达的患者接受戈沙妥珠单抗(SG)治疗相比化疗PFS和OS全面获益,但高表达组明显获益更加明显(图6)[10]。。可见,Trop-2表达水平的检测在Trop2靶向药物的开发中至关重要,相关的免疫组化检测及其伴随诊断产品开发很可能会加速Trop-2药物的上市进程和适应症的扩展。
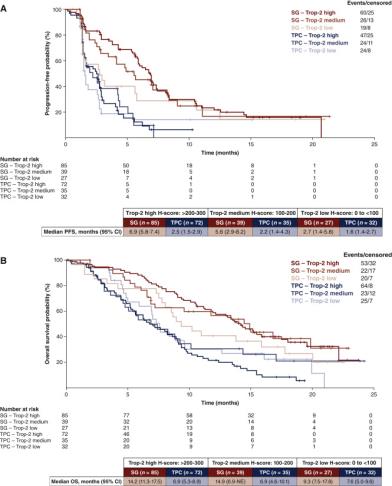
图6.Trop-2表达与PFS、OS的关系
Trop-2检测方法简介
质控选择
在人体正常组织和肿瘤组织中,使用IHC检测Trop-2表达,可以看到染色主要定位于细胞膜,部分伴有较弱的细胞质染色[4]。扁桃体可同时作为阴阳性对照使用,作为阳性对照时,扁桃体隐窝上皮表现出较强的膜染色;作为阴性对照时,除扁桃体隐窝上皮外的其他区域应为阴性。选取皮肤作为阳性对照时,皮肤的表皮细胞应表现出较强的膜染色。
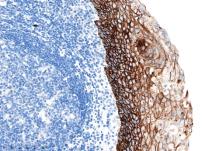
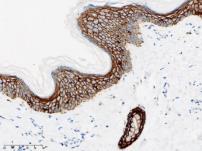
Trop-2扁桃体染色 Trop-2皮肤染色
(来自熙宁生物IHC实验室)
评分方法
在ASCENT研究中,Trop-2的高、中、低表达通过组织化学评分(H-score)方法来进行判读,将每张切片内阳性的细胞数量及其染色强度转化为相应的数值,从而达到对组织染色半定量的目的。据此我们建立起了Trop-2的判读方式标准(如下表所示)。
|
染色强度 |
对应染色强度的肿瘤占比 |
结果计算 |
分组标准 |
|
1+ |
A |
H=1×A+2×B+3×C (范围0~300)
|
低表达组H<100; 中表达组H=100~200; 高表达组H>200 |
|
2+ |
B |
||
|
3+ |
C |
|
|
|
|
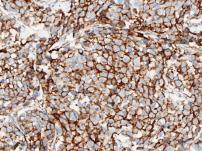
染色评分3+ |
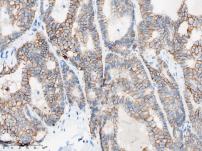
染色评分2+ |
|
|
|
|
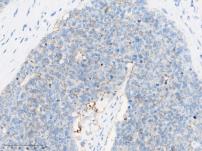
染色评分1+ |
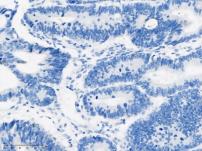
染色评分0 |
Trop-2染色等级示意图(来自熙宁生物IHC实验室)
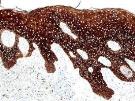
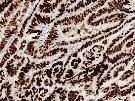
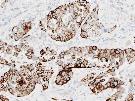
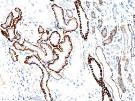
总之,熙宁生物IHC实验室目前已建立了成熟的Trop-2染色方法与判读体系,适用乳腺癌、胃癌、肺癌等多个癌种,可快速用于相关肿瘤的临床试验入组筛选与样本检测。同时,熙宁生物也在积极布局Trop-2 IHC伴随诊断试剂盒的开发工作,部分结果展示如图所示,欢迎广大药企客户垂询,共同进行Trop-2 伴随诊断产品的定制开发。
熙宁生物致力于为国内外生物制药企业提供国际质量标准的大分子生物分析和伴随诊断开发服务,期待与众多创新药企鼎力合作,助力Trop-2药物的研发与上市,给患者带来新的治疗机会。
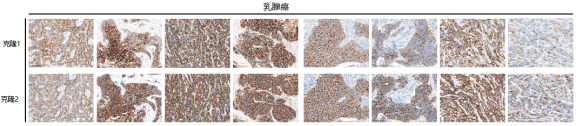
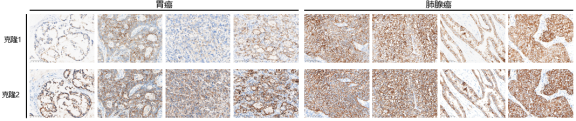
Trop-2染色(来自熙宁生物IHC实验室)
关于熙宁生物免疫组化检测服务
熙宁生物免疫组化平台拥有BenchMark Ultra,Dako Autostainer Link 48等国际公认的免疫组化染色平台,遵从CAP和GCP要求,按照“合规,精准,伴随诊断”的理念,成功完成包括PD-L1、Claudin18.2、dMMR、TIM-3、TROP-2、AR等超过50种靶标的免疫组化方法开发,其中多种检测方法已获得国内外权威机构NordiQC, CCPI 等的认可。对于客户的伴随诊断产品开发需求,我们也筛选出了多株有伴随诊断开发价值的单克隆抗体,可随时为广大药企客户提供方法学开发,样品检测,抗体筛选,伴随诊断试剂盒定制化开发等服务。
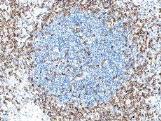
|
扁桃体 |
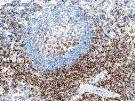
|
CD4 |
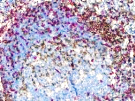
|
CD4(棕色)/CD8(红色) |
|
Her-2 |
|
ER |
|
Nectin-2 |
|
NY-ESO-1 |
|
TIGIT |
|
PVR |
|
扁桃体PD-L1 |
|
肺癌PD-L1 |
|
肺癌PD-L1 |
|
Claudin18.2 |
|
CD276(B7-H3) |
|
Ki-67 |
|
PD-1 |
|
MLH1 |
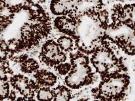
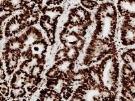

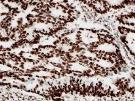
|
MSH2 |
|
PMS2 |
|
MSH6 |
|
TIM-3 |
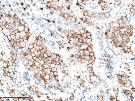
|
K16 |
|
p53 |
|
CK5 |


|
EpCAM |
|
CD31 |
|
CD45 |
|
CD47 |

|
Trop-2 |
|
AR |

|
CD8 |

|
CD3 |
|
扁桃体 |
参考文献
[1]. Rettig WJ, Cordon-Cardo C, Koulos JP, Lewis JL Jr, Oettgen HF, Old LJ. Cell surface antigens of human trophoblast and choriocarcinoma defined by monoclonal antibodies. Int J Cancer. 1985 Apr 15;35(4):469-75.
[2]. Goldenberg DM, Stein R, Sharkey RM. The emergence of trophoblast cell-surface antigen 2 (TROP-2) as a novel cancer target. Oncotarget. 2018 Jun 22;9(48):28989-29006.
[3]. Lenárt S, Lenárt P, Šmarda J, Remšík J, Souček K, Beneš P. Trop2: Jack of All Trades, Master of None. Cancers (Basel). 2020 Nov 11;12(11):3328.
[4]. Stepan LP, Trueblood ES, Hale K, Babcook J, Borges L, Sutherland CL. Expression of Trop2 cell surface glycoprotein in normal and tumor tissues: potential implications as a cancer therapeutic target. J Histochem Cytochem. 2011 Jul;59(7):701-10.
[5].Trerotola M, Cantanelli P, Guerra E, Tripaldi R, Aloisi AL, Bonasera V, Lattanzio R, de Lange R, Weidle UH, Piantelli M, Alberti S. Upregulation of Trop-2 quantitatively stimulates human cancer growth. Oncogene. 2013 Jan 10;32(2):222-33.
[6]. Liao S, Wang B, Zeng R, Bao H, Chen X, Dixit R, Xing X. Recent advances in trophoblast cell-surface antigen 2 targeted therapy for solid tumors. Drug Dev Res. 2021 Dec;82(8):1096-1110.
[7]. Zaman S, Jadid H, Denson AC, Gray JE. Targeting Trop-2 in solid tumors: future prospects. Onco Targets Ther. 2019 Mar 1;12:1781-1790.
[8]. Zeng P, Chen MB, Zhou LN, Tang M, Liu CY, Lu PH. Impact of TROP2 expression on prognosis in solid tumors: A Systematic Review and Meta-analysis. Sci Rep. 2016 Sep 20;6:33658.
[9]. Shvartsur A, Bonavida B. Trop2 and its overexpression in cancers: regulation and clinical/therapeutic implications. Genes Cancer. 2015 Mar;6(3-4):84-105.
[10].Bardia A, Tolaney SM, Punie K, Loirat D, Oliveira M, Kalinsky K, Zelnak A, Aftimos P, Dalenc F, Sardesai S, Hamilton E, Sharma P, Recalde S, Gil EC, Traina T, O'Shaughnessy J, Cortes J, Tsai M, Vahdat L, Diéras V, Carey LA, Rugo HS, Goldenberg DM, Hong Q, Olivo M, Itri LM, Hurvitz SA. Biomarker analyses in the phase III ASCENT study of sacituzumab govitecan versus chemotherapy in patients with metastatic triple-negative breast cancer. Ann Oncol. 2021 Sep;32(9):1148-1156.
[11]. Gao XY, Zhu YH, Zhang LX, Lu HY, Jiang AG. siRNA targeting of Trop2 suppresses the proliferation and invasion of lung adenocarcinoma H460 cells. Exp Ther Med. 2015 Aug;10(2):429-434.
咨询
- 221
- 点赞
- 复制链接
- 举报