Mol Cancer. (Q1,41.444)|结直肠癌外泌体CircLPAR1抑制METTL3-eIF3h互作降低BRD4水平


外泌体是多种癌症的重要生物标志物,外泌体富含环状RNA(circRNA)。然而,外泌体circRNA用于诊断的潜力及其在结直肠癌(CRC)中的分子作用机制仍不清楚。
通过RNA测序、exoRBase数据库和组织芯片鉴定CRC特异性外泌体circRNA。在癌旁对照、癌前个体、CRC患者和其他类型癌症患者中评估了血浆外泌体circRNA的诊断性能。主要使用circRNA pull-down、蛋白质组学分析和基于细胞和小鼠模型的RNA免疫沉淀测定来评估相应的生物学功能。
CircLPAR1是外泌体中具有高稳定性和可检测性的环状RNA分子,其表达在CRC发展过程中患者血浆外泌体中显著降低,且手术后恢复。通过结合常见的临床生物标志物CEA和CA19-9分析其性能,外泌体circLPAR1在CRC诊断中显示出癌症特异性,并将诊断性能提高ROC曲线0.875的区域。此外,circLPAR1在CRC组织中下调,并与总生存期相关。从机制上讲,外泌体circLPAR1被CRC细胞内化,它抑制了肿瘤生长,可能是因为外泌体circLPAR1直接与eIF3h结合,特异性抑制了METTL3-eIF3h的相互作用,从而降低了致癌基因BRD4表达。
这项综合性研究强调了血浆外泌体circLPAR1可作为CRC诊断的高灵敏预测因子,并描述了其对结直肠肿瘤发生的生物学调节。该研究为临床早期诊断和疾病发展中的发病机制提供了新的视角。
结直肠癌已成为消化系统最常见的恶性肿瘤之一,近年来,我国结直肠癌的发病率和死亡率居高不下。尽管结肠镜检查、结肠镜检查和基于粪便的检测等方法已应用于临床,但结直肠癌的早期发现和诊断仍然具有极高挑战性。
外泌体被认为是一类非常有前景的生物标志物来源。大量证据表明,外泌体通过将源自亲代细胞的特定物质递送至参与疾病发展和进展的受体细胞,在细胞间通讯中充当信使。环状RNA(circRNA)已被证明在外泌体中明确富集,此外,circRNA可以在各种组织和体液的病理条件下特异性和差异表达,包括结直肠癌,因此可作为疾病进展的潜在生物标志物用于诊断。目前,很少有研究报道外泌体circRNA在结直肠癌中的诊断作用。
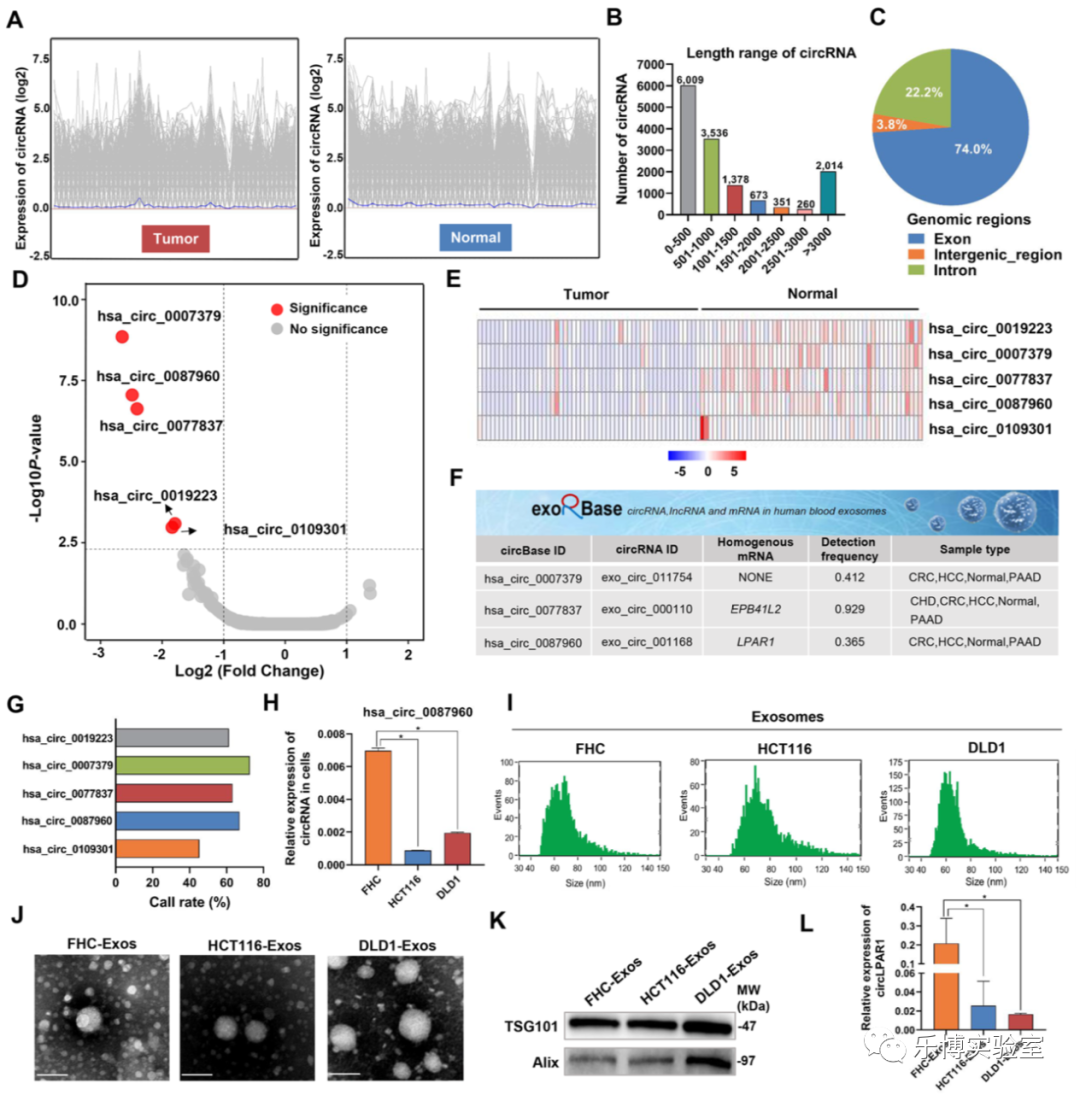
为了研究结直肠癌中circRNA的表达谱,对52对结直肠肿瘤和正常癌旁组织(NATs)样品进行了RNA-Seq,共检测到14,221个circRNA,它们大部分小于500nt,70%以上来源于蛋白质编码外显子,其次是内含子和基因间区域。并筛选出5个显著降低的差异circRNA分子(hsa_circ_0019223、hsa_circ_0007379、hsa_circ_0077837、hsa_circ_0087960和hsa_circ_0109301)。exoRBase数据库注释后发现三个外泌体circRNA(hsa_circ_0007379、hsa_circ_0077837和hsa_circ_0087960)高丰度表达,而hsa_circ_0087960(circLPAR1)是唯一在结直肠癌细胞(HCT116和DLD1)中表达显著下调。从细胞培养基(FHC-Exos和HCT116/DLD1-Exos)中纯化外泌体并观察到典。此外,用外泌体分泌抑制剂GW4869处理后,细胞培养基中的circLPAR1水平显著降低
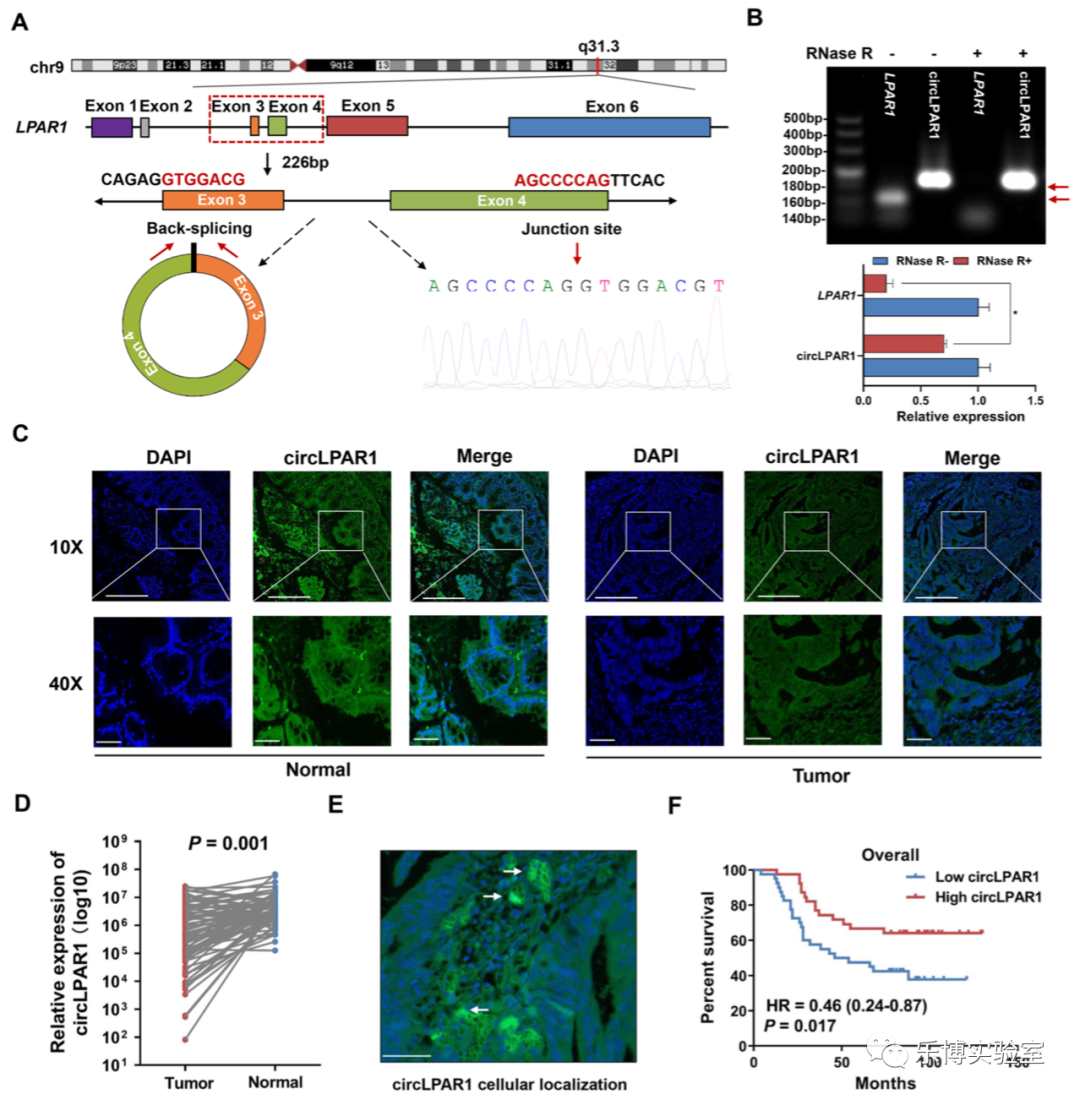
CircLPAR1由位于chr9 (113734352-113735838)上的LPAR1基因的3号外显子和4号外显子环化产生,长226 bp,具有“头对尾”反向剪接位点,放线菌素D(一种转录抑制剂)处理结肠直肠癌细胞,并观察到circLPAR1比线性LPAR1转录物更稳定,且circLPAR1对 RNase R 消化(线性RNA的降解剂)具有抗性。FISH 测定也证实了RNA-Seq数据。circLPAR1主要在细胞质中表达和定位,circLPAR1高表达水平的结直肠癌患者的总生存期更优于circLPAR1低水平患者。
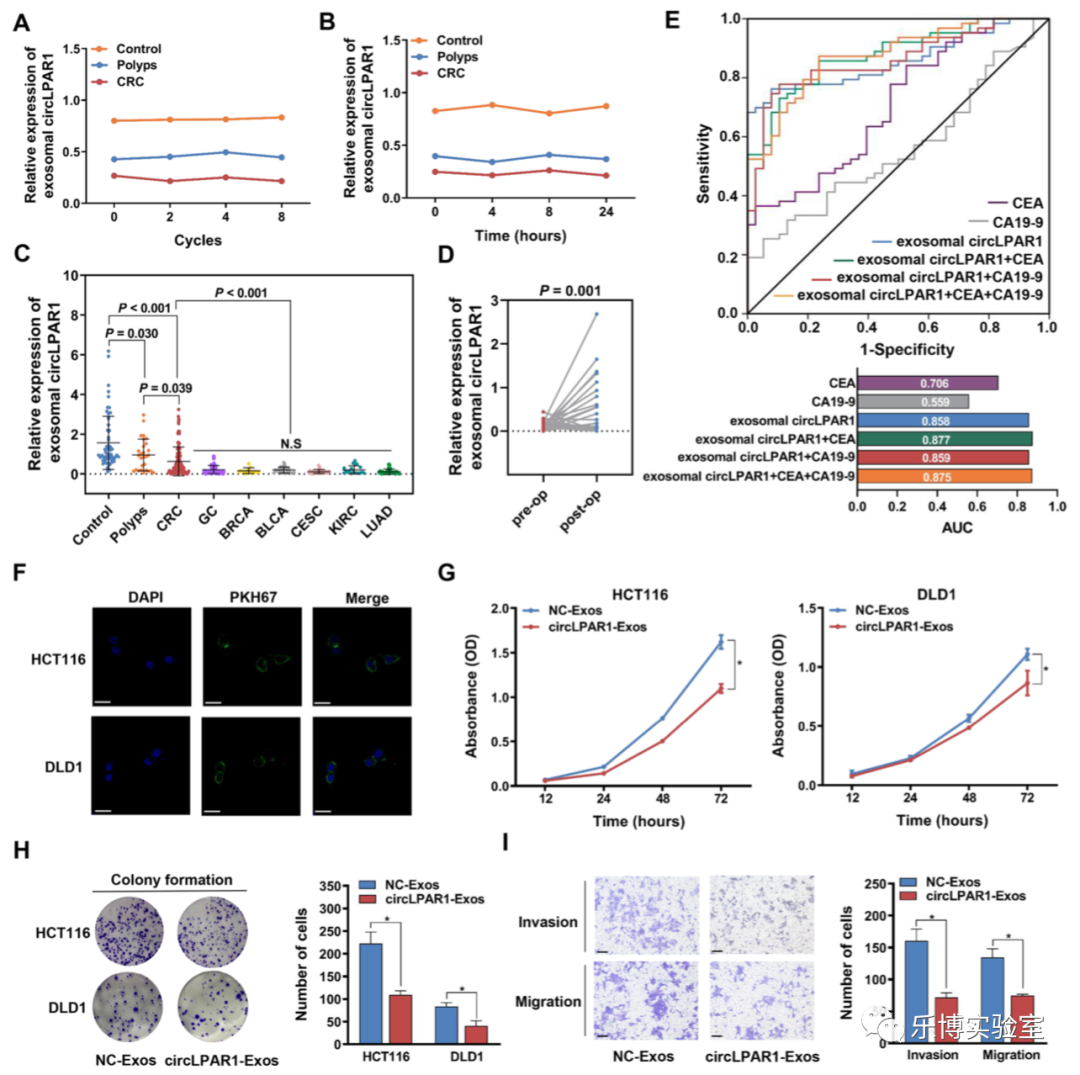
通过分析血浆中分离物形态、标记表达和大小成功地鉴定了血浆外泌体。并观察到血浆中外泌体circLPAR1表达水平在经过反复冻融或在室温下放置不同时间均没有显著影响。与癌旁相比,结直肠癌患者的外泌体circLPAR1显著降低。结直肠肿瘤切除后外泌体circLPAR1水平显著升高,ROC曲线显示,外泌体circLPAR1可以作为一个高灵敏性和特异性的分子以区分结肠直肠癌患者其AUC面积为0.858,显著高于目前CEA和CA19-9(CEA:AUC=0.706;CA19-9:AUC=0.559,目前广泛用于结直肠癌诊断的临床生物标志物),当外泌体circLPAR1、CEA和CA19-9联合使用时AUC值增加到0.875,灵敏性和特异性分别为87.30和76.30%。
接下来,文章探索了外泌体circLPAR1在结直肠肿瘤发生中的生物学功能。荧光显微镜显示HCT116和DLD1细胞的细胞质中有PKH67绿色荧光染料,而非Exos组未观察到,提示HCT116/DLD1-Exos被细胞迅速吞噬,然而,这种摄取被细胞松弛素D抑制内吞作用所消除。转染circLPAR1/NC载体(circLPAR1/NC-Exos)的结直肠癌细胞中分离出外泌体,发现直接与circLPAR1-Exos孵育显著增加了HCT116和DLD1细胞中的circLPAR1水平。此外,观察到外泌体circLPAR1显著抑制了结直肠癌细胞的增殖、集落形成、侵袭和迁移。这一发现与circLPAR1过表达获得的结果相似。
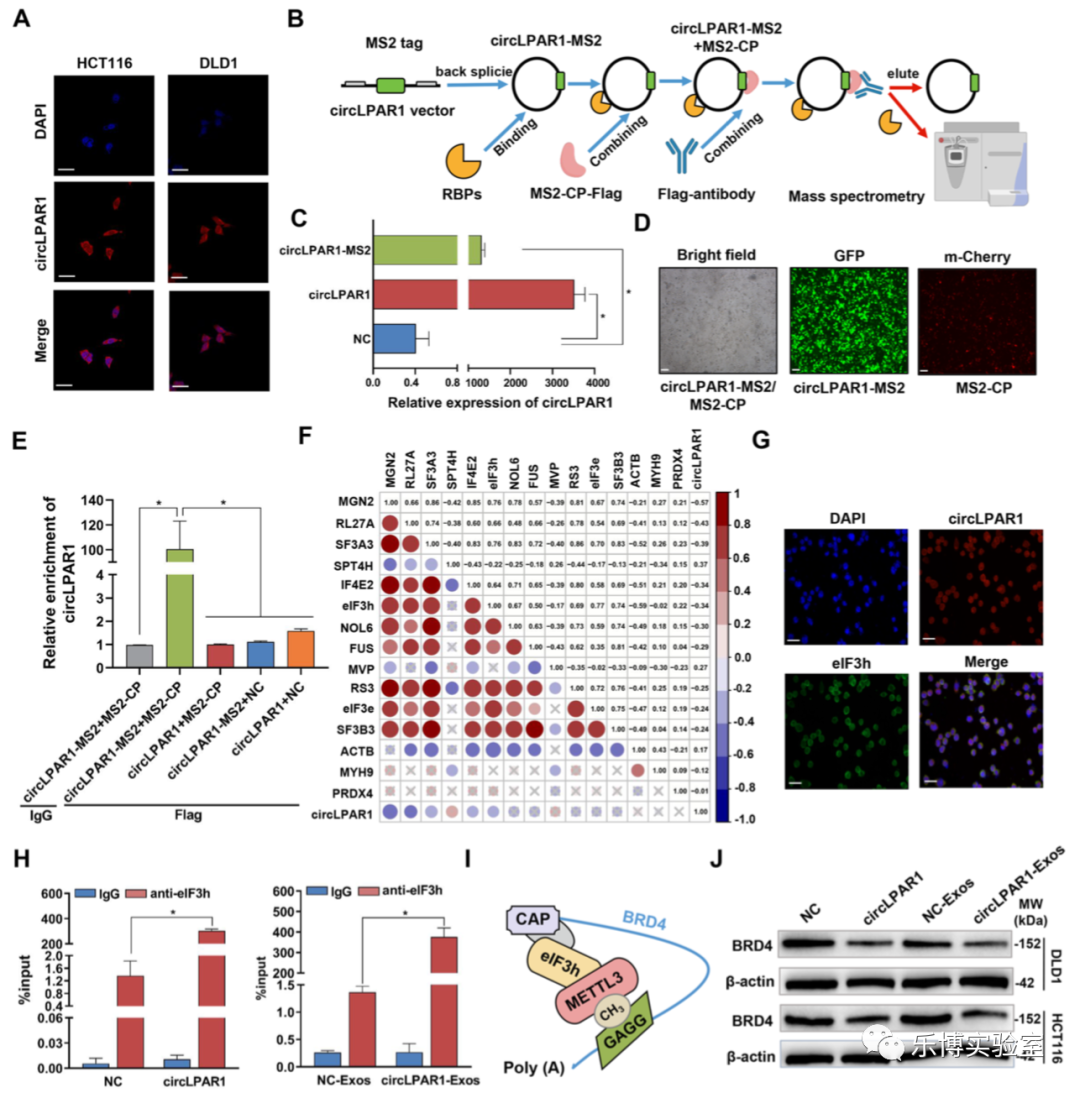
CircLPAR1 在细胞系和组织的细胞质中均富集,于是作者将关注点落到circLPAR1 影响的特定 circRNA-RBP 复合物上。通过 MS2-CP-Flag circRNA pull-down最终共鉴定了 23 个circLPAR1 的候选 RBP。随后基于 25 对结直肠肿瘤和 NAT 进一步检测这些 RBP 的蛋白表达,发现肿瘤中 12 个 RBPs 被上调,3 个 RBPs 被下调。此外,circLPAR1 与 6 个 RBP(MGN2、RL27A、SF3A3、SPT4H、IF4E2 和 eIF3h)显著相关,其中 4 个 RBP(MGN2、RL27A、SF3A3和 eIF3h)与其亲本线性 RNA 呈正相关。此外,通过用 catRAPID 签名/表达模块估计了这四种特异性针对 circLPAR1 的 RBP 的结合能力,发现 eIF3h 与 circLPAR1 的结合能力最强。
为了确认circLPAR1对eIF3h的结合力,首先观察它们并确定了circLPAR1和eIF3h在结直肠癌细胞细胞质中的共定位。RIP 实验进一步证实,circLPAR1 或外泌体 circLPAR1 直接与eIF3h特异性结合。有报告称,eIF3h 与甲基转移酶样 3 (METTL3) 之间存在直接的物理和功能相互作用,可调节含溴结构域蛋白 4 (BRD4) 的翻译并影响肿瘤发生。与NC/NC-Exos组相比,circLPAR1慢病毒载体转染或circLPAR1-Exos孵育的结直肠癌细胞中的BRD4蛋白水平降低,为了排除 circLPAR1 对 BRD4调节作用,将 BRD4 表达载体转染到稳定的 circLPAR1 表达细胞中,然后用特异性 BRD4 抑制剂 AZD5153 处理。BRD4表达质粒提高了由circLPAR1表达引起的BRD4水平的降低,并促进了结直肠癌细胞相关表型,而AZD5153逆转了高BRD4水平的促肿瘤作用。
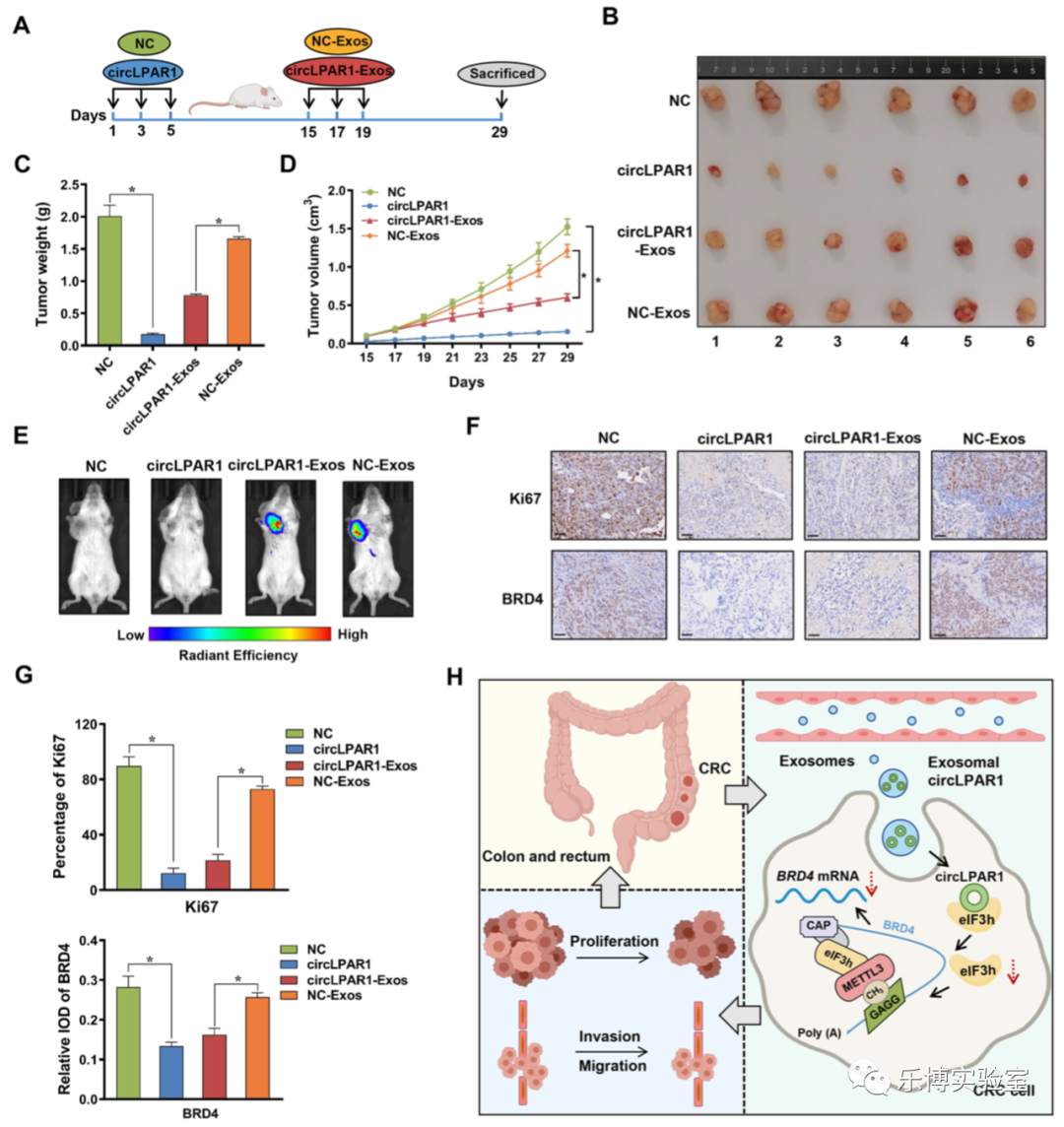
为了验证体内外泌体circLPAR1在结直肠癌中的抑制作用,将circLPAR1/NC过表达细胞或DiR染色的circLPAR1/NC-Exos构建人源化NCG小鼠模型。与体外结果一致,与NC表达或NC-Exos治疗相比,circLPAR1过表达或circLPAR1-Exos治疗降低了肿瘤的大小和重量。circLPAR1和circLPAR1-Exos组的肿瘤生长更慢,实时成像结果还显示,DiR染色的circLPAR1/NC-Exos被成功注射到小鼠体内。与NC/NC-Exos组相比,circLPAR1或circLPAR1-Exos组的肿瘤具有更高水平的circLPAR1。此外,HE染色和IHC染色分析显示circLPAR1和circLPAR1-Exos组的Ki67和BRD4受损。
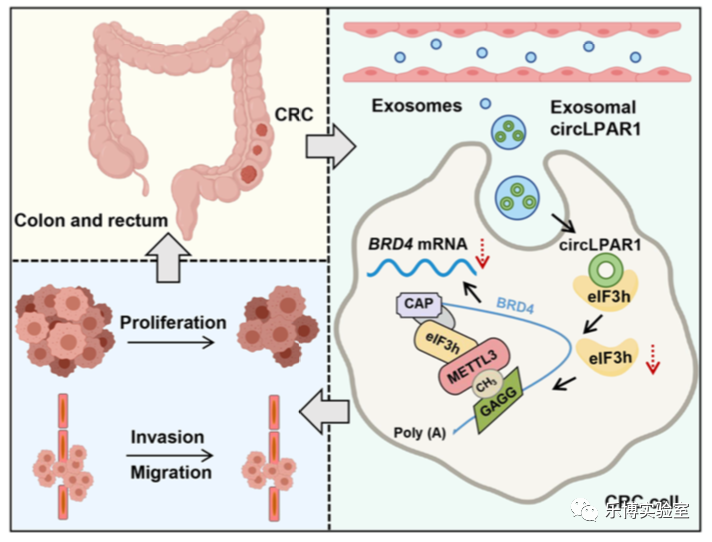
本研究确定了一种新的结直肠癌相关circRNA分子,叫外泌体circLPAR1,可从血浆分离外泌体中检测,并可能能作为健康体检或结直肠癌症的早期筛查的一种高特异性和灵敏性的生物标志物。从机制上讲,外泌体circLPAR1结合eIF3h并抑制METTL3-eIF3h相互作用,导致BRD4水平降低,从而显著抑制结直肠癌的发展。不仅报道了外泌体circRNA在结直肠癌中的新机制,而且为结直肠癌的筛查策略和诊断方法开辟了新视角。
咨询
- 280
- 点赞
- 复制链接
- 举报