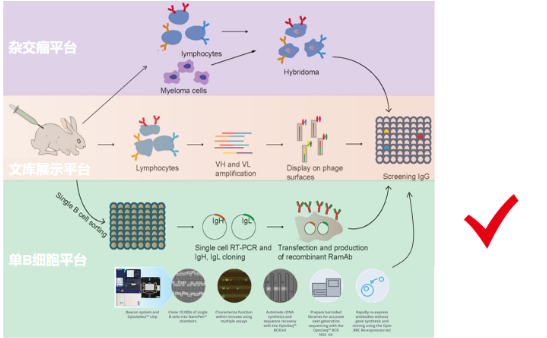
肿瘤免疫靶点|免疫检查点LAG-3
从PD-1/PD-L1开始,开启了免疫检查点抑制剂治疗癌症治疗的新征程。随着对免疫检查点研究的深入,针对多个免疫检查点都开展了研究,包括CTLA-4,LAG-3,TIM-3和TIGIT。本文主要介绍LAG-3。
LAG-3
分子别名:淋巴细胞活化基因3(Lymphocyte-activation gene 3,LAG-3),又称为CD233
发现:1990年由Triebel及其同事发现,在活化的人类NK和T细胞系上被鉴定出来。
家族:LAG-3是属于免疫球蛋白(Ig)超家族的I型跨膜蛋白。
表达:活化的T细胞、NK细胞、B细胞和浆细胞样DC中表达。LAG3的表达是通过TCR或细胞因子(IL-12、IL-27、IL-15、IL-2和IL-7)的激活而诱导的。在多种肿瘤中,LAG-3都与较差的预后相关。
配体:已经发现了的发现了配体包括:MHC II分子,肝窦内皮细胞凝集素(LSECtin),galectin-3,α-synuclein,FGL-1。
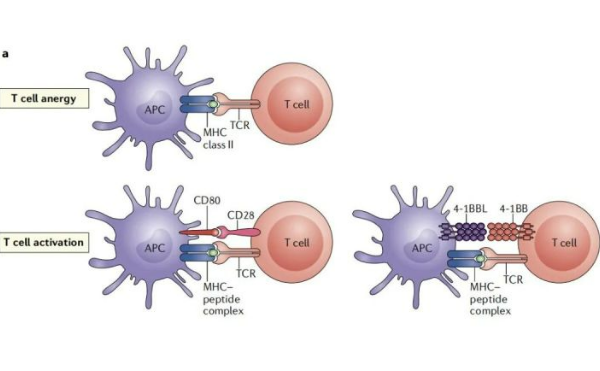
功能:LAG-3抑制T细胞的激活和细胞因子的分泌,从而保证免疫稳态。LAG3能够调控T淋巴细胞和抗原呈递细胞(APCs)的信号通路,在适应性免疫反应中起到重要作用。与肿瘤、结核等多种疾病相关。
发现:1990年由Triebel及其同事发现,在活化的人类NK和T细胞系上被鉴定出来。
家族:LAG-3是属于免疫球蛋白(Ig)超家族的I型跨膜蛋白。
表达:活化的T细胞、NK细胞、B细胞和浆细胞样DC中表达。LAG3的表达是通过TCR或细胞因子(IL-12、IL-27、IL-15、IL-2和IL-7)的激活而诱导的。在多种肿瘤中,LAG-3都与较差的预后相关。
配体:已经发现了的发现了配体包括:MHC II分子,肝窦内皮细胞凝集素(LSECtin),galectin-3,α-synuclein,FGL-1。
功能:LAG-3抑制T细胞的激活和细胞因子的分泌,从而保证免疫稳态。LAG3能够调控T淋巴细胞和抗原呈递细胞(APCs)的信号通路,在适应性免疫反应中起到重要作用。与肿瘤、结核等多种疾病相关。
从PD-1/PD-L1开始,开启了免疫检查点抑制剂治疗癌症治疗的新征程。随着对免疫检查点研究的深入,针对多个免疫检查点都开展了研究,包括CTLA-4,LAG-3,TIM-3和TIGIT。本文主要介绍LAG-3。
LAG-3结构
LAG-3由胞外区、跨膜区和胞质区3部分组成,共含498个氨基酸。
胞外区:由四个Igg样胞外结构域组成:D1、D2、D3和D4。
D1: LAG3的D1结构域位于膜远端,它有一个富含脯氨酸的独特的环状结构(约包含30个氨基酸),这是LAG-3与MHC II类分子结合的关键位点。该区域的点突变可以增强或减少与MHCII的结合,而缺失则会完全破坏MHCII的结合。这个环状结构也是阻断LAG3:MHCII相互作用的抗体的结合表位。
D2: D2结构域起到定位D1结构域与MHC II结合的位置,D1和D2都是LAG3与MHCII结合的必要和充分条件。LAG3中D3-D4域的缺失并不影响FGL1的结合,而D1或D2单独都部分降低了FGL1与LAG3的结合,表明D1和D2都参与了FGL1/LAG3的相互作用。
D4: D4结构域位于胞外近膜端,在穿膜金属蛋白酶ADAM10和ADAM17的作用下,D4和跨膜区之间的连接肽断裂形成可溶性LAG3(sLAG3)。
(数据来源:Fibrinogen-like Protein 1 Is a Major Immune Inhibitory Ligand of LAG-3)
胞质区:丝氨酸磷酸化位点、“KIEELE”基序和谷氨酸-脯氨酸双肽重复基序(EP序列)。
丝氨酸磷酸化位点是蛋白激酶C(PKC)的底物。EP序列和KIEELE基序为高度保守序列。其中KIEELE基序具有特异性,其参与LAG-3胞内信号转导,这对LAG-3调节T细胞功能起到关键作用。
LAG-3配体
MHC II分子:MHC II分子为LAG-3的主要配体,MHC II类,由抗原呈递细胞或黑素瘤细胞异常表达,与LAG3结合,然后通过LAG-3胞质区域传递抑制信号。
LSECtin:LSECtin(肝窦内皮细胞凝集素)属于C型凝集素受体超家族,是II穿膜蛋白。它在肝脏和黑色素瘤细胞中高表达。通过与LAG-3的相互作用抑制CD8+T细胞和NK细胞免疫应答。
Galectin-3:Galectin-3(半乳糖凝集素-3)是一种可以结合半乳糖苷的可溶性凝集素,大小为31 kDa。在肿瘤微环境中,Galectin-3被许多细胞表达,而不是肿瘤细胞本身,它可与糖基化的LAG-3相互作用,可以抑制CD8+T细胞的细胞毒性。
α-synuclein:像MHCII一样,α-synuclein结合到LAG-3 D1区域,并依赖于D2, D3或细胞内结构域。
FGL-1:FGL1(纤维蛋白原样蛋白1)在肝脏(低水平)和肿瘤细胞中(高水平)表达。FGL1是LAG3的高亲和力配体。FGL1与LAG-3相互可以促进肿瘤免疫逃逸。阻断FGL-1-LAG-3通路可以增强CD8+T细胞抗肿瘤作用。在LAG3 D1结构域的一个单点突变(Y73F)之前被证明会破坏MHC-II结合。然而,该突变并不影响FGL1-Ig结合。表明FGL1与LAG3以MHC-II独立的方式相互作用。
LAG-3作用机制
LAG3胞质结构域的EP基序可与LAG3相关蛋白(LAP)结合。LAG3胞质中的kieele基序在所有灵长类动物、小鼠和大鼠之间都是保守的。该序列中的单个赖氨酸残基(小鼠中为Lys468)是不可缺少的,并且在迄今为止测序的所有物种中都是保守的。
在配体结合时,LAG3以依赖于LAG3胞质结构域的方式抑制TCR通路,阻止了包括NFAT在内的转录因子的激活,从而减少了细胞因子的产生和增殖。
(数据来源:Graydon Colin G,Mohideen Shifa,Fowke Keith R,LAG3's Enigmatic Mechanism of Action)
靶向LAG-3的抗体对免疫细胞的影响
LAG-3对CD4+T细胞、CD8+T细胞、NK细胞、pDCs起负向调控的作用,LAG-3促进Tregs细胞的抑制活性。
(数据来源:The promising immune checkpoint LAG-3: from tumor microenvironment to cancer immunotherapy)
LAG-3相关药物
以LAG-3为靶点的药物主要治疗领域包括癌症和自身免疫性疾病。
靶向LAG3药物分为几类:拮抗性抗体,激动剂抗体,双特异性抗体,APC激活剂。
目前BMS的relatlimab、默沙东的favezelimab和MacroGenics的双抗tebotelimab三款抗体处于靶向LAG-3研发的前列。
拮抗性抗体
百时美施贵宝(BMS)Relatlimab
PD-1和PD-L1治疗在部分晚期恶性肿瘤患者中有效。然而,一个问题是:大多数患者对它没有反应。而抗LAG-3和抗PD-1联合免疫疗法在对抗PD-1耐药性方面显示出令人兴奋的疗效。
第一个进入临床的LAG-3抑制性单抗是Relatlimab,它是一种IgG4亚型的全人源抗体。它阻断了LAG-3与MHCⅡ的相互作用。
在2021年的ASCO大会上,BMS公司公布了其LAG-3抗体Relatlimab与PD-1抗体纳武单抗联合用于治疗晚期黑色素瘤的试验结果:
355名接受relatlimab+纳武单抗治疗的患者,中位无进展生存期10.1个月,1年无进展生存率47.7%;
359名接受纳武单抗单药治疗的患者,中位无进展生存期4.6个月,1年无进展生存率36.0%;
同时,Relatlimab的加入让晚期黑色素瘤患者疾病进展的风险降低了25%。
2021年9月20日,百时美施贵宝宣布FDA受理LAG-3抗体Relatlimab的上市申请,并授予优先审评资格,适应症为用于和PD-1抗体Nivolumab联合治疗转移性不可切除的黑色素瘤。它有望成为第一个上市的LAG-3抗体,开辟一类新的免疫治疗药物。
(数据来源:ASCO2021)
默沙东Favezelimab
Favezelimab是默沙东公司开发的一款在研LAG-3抗体,能够阻断MHCII类受体与LAG-3之间的相互作用,抑制LAG-3上调,进而恢复T细胞对肿瘤细胞的杀伤效应。
2021年7月28日,中国国家药品监督管理局药品审评中心(CDE)网站公示显示,默沙东(MSD)的1类新药MK-4280A注射液临床试验申请获得受理。
MK-4280A是LAG-3抗体favezelimab(MK-4280)和PD-1抑制剂Keytruda的联合治疗方案。Keytruda是一款PD-1抑制剂。
以上药物都属于LAG3的拮抗性抗体,通过阻断LAG3与其配体的结合而阻断LAG-3介导的对T细胞的抑制信号。拮抗性LAG3抗体既可激活效应T细胞,也可以抑制Treg活性。而其他检查点靶点(例如PD-1 / PD-L1和CTLA-4)仅能激活效应T细胞,所以这种具有双重作用机制的LAG3成为检查点抑制的重要靶点。
诺华公司-LAG525
LAG525 (INN: leramilimab或IMP701)是由诺华公司(Novartis)开发的一种拮抗单克隆抗体(mAb),它阻断了LAG-3介导的肿瘤浸润T细胞的抑制信号。这使得CD8 T细胞对癌细胞产生更好的细胞毒性反应。该候选产品目前正在不同的II期临床试验中。
(数据来源:Immutep: https://www.immutep.com/technology/lag-3-technology.html)
恒瑞:SHR-1802
SHR-1802是恒瑞开发的一款抗LAG-3单抗。2019年11月18日,恒瑞医药注射用SHR-1802获得临床试验默示许可,适应症为标准治疗失败的晚期恶性肿瘤(NCT04414150),目前,该药物还处于临床Ⅰ期。
信达生物:IBI110
IBI110是信达生物开发的一款新型抗LAG-3抗体,已在中国获批临床,拟开发用于治疗血液癌症和实体瘤。根据中国药物临床试验登记与信息公示平台信息,信达生物正在开展一项开放性1期研究,以评估IBI110单药及联合PD-1抑制剂信迪利单抗治疗晚期恶性肿瘤受试者的安全性、耐受性和有效性。
维立志博:LBL-007
LBL-007是维立志博开发的一种IgG4亚型全人源单克隆抗体,可通过结合人LAG-3蛋白来阻断LAG-3蛋白与其配体的结合,从而解除LAG-3对T细胞的抑制作用,使T细胞恢复免疫功能,起到对肿瘤生长的抑制作用。
维立志博正在开展两项1期临床试验:
●评估LBL-007联合PD-1抑制剂特瑞普利单抗一线治疗不可切除或转移性黑色素瘤的安全性、耐受性、有效性;
●评估LBL-007在晚期实体瘤和晚期淋巴瘤患者中的安全性、耐受性、药代动力学及有效性。
时迈药业:DNV3
DNV3是时迈药业开发的一款抗LAG-3单抗。临床前药效学研究显示,DNV3可精准调控包括T细胞、B细胞、自然杀伤(NK)细胞及树突状细胞(DC)等多类免疫细胞的功能,单药治疗具有显著抗肿瘤药效。同时,DNV3与化疗、小分子靶向药及PD-1免疫检查点抑制剂联用可进一步协同提高抗肿瘤药效。2020年8月,DNV3在中国获批一项临床默示许可,拟开发用于晚期/转移性实体瘤和淋巴瘤治疗。
双特异性抗体
再鼎医药:MGD013
MGD013(tebotelimab)是一种能够同时与PD-1和LAG-3相结合的双特异性抗体。它是利用Macrogenics公司的DART®平台开发的双特异性抗体,旨在提高分子稳定性,延长抗体的半衰期。2018年11月,再鼎医药与MacroGenics公司达成合作,获得了MGD013在大中华区的开发及商业化授权。MGD013在血清中的半衰期很长。据预测,Tebotelimab可以用于治疗包含多种实体瘤和血液系统恶性肿瘤在内的广泛癌症类型。Tebotelimab的I期剂量递增研究正在进行。
目前,再鼎在国内开展了MGD013单药,以及联合HER2抗体(HER2+GC/GEJ,II/III期)、PARP抑制剂(晚期GC、TNBC、胆管/胆囊癌等)、VEGFR2抑制剂(肝细胞癌)等多个临床研究。
岸迈生物:EMB-02
EMB-02是岸迈生物开发的一款PD-1和LAG-3的双特异性抗体。在对PD-1抗体单药治疗耐药的临床前模型中,EMB-02已显示出了显著的抗肿瘤活性。EMB-02的1/2期临床试验是一项多中心、开放、多剂量的人体临床研究,旨在评估 EMB-02 在晚期实体瘤患者中的安全性和耐受性。临床1期的首要目标是确定药物在临床2期推荐剂量 (RP2D) 和安全时间。同时会评估 EMB-02 的药代动力学、免疫原性和抗肿瘤活性。
信达生物:IBI323
从PD-1/PD-L1开始,开启了免疫检查点抑制剂治疗癌症治疗的新征程。随着对免疫检查点研究的深入,针对多个免疫检查点都开展了研究,包括CTLA-4,LAG-3,TIM-3和TIGIT。本文主要介绍LAG-3。
(数据来源: PD-L1/LAG-3 bispecific antibody enhances tumor-specific immunity)
相对于亲本抗体BI127,IBI323对PD-L1的结合亲和力保持不变。
BI127在Fc部分引入LALA突变(LALA, L234A, L235A),降低了Fc介导的抗体依赖细胞介导的毒性(ADCC)和补体介导的细胞毒性。
它同时抑制LAG-3和PD-L1介导的两个抑制性信号通路,比单靶点更强且更持久的T细胞活化潜力。它可以将表达PD-L1的肿瘤细胞与表达LAG-3的T细胞拉近,从而形成稳定的TCR:MHC免疫突触,进一步激活T细胞。CIBI323A101是一项在中国开展的评估IBI323治疗标准治疗失败的晚期恶性肿瘤受试者的安全性、耐受性和抗肿瘤活性的I期研究(NCT04916119)。
ABL Bio:ABL501
ABL501是一种双特异性抗体,可阻断PD-L1和LAG-3检查点通路,以克服目前PD-(L)1治疗的局限性。ABL501是一种全长抗LAG-3单抗,融合了PD-L1单抗的scFv。ABL501表现出比单一疗法和联合疗法更好的活性。目前处于临床Ⅰ期,适应症为晚期实体瘤。
LAG3的激动剂抗体
IMP761是一种LAG-3激动剂抗体。它是一种人源化IgG4单克隆抗体。
使用针对被激活的T细胞表面的LAG-3受体的激动剂抗体,可以直接向T细胞传递更强的抑制信号,从而阻止T细胞继续增殖,并对患者的组织产生反应。IMP761的临床发展我们的目标是解决自身免疫性疾病的根源,IMP761的临床发展我们的目标是解决自身免疫性疾病的根源。目前,该候选产品还处于临床前阶段。
APC激活剂
Eftilagimod alpha(IMP321)是一种重组蛋白,由一种LAG-3的二聚体组成的可溶性LAG-3,它与APC表面的主要组织相容性复合体(MHC) II类分子结合,导致抗原呈递细胞(如单核细胞和树突状细胞)的激活,进一步导致细胞毒性CD8+ T细胞数量和激活的生理增加,是一种积极的免疫治疗机制。通过这些作用机制,可溶性的LAG-3(如IMP321/eftilagimod alpha)可以增加对癌症抗原的免疫应答。目前正处于癌症治疗的晚期临床开发阶段。目前为止,IMP321作为单一疗法并未显示出显著的疗效,但作为联合疗法具有前景。
(数据来源:Immutep: https://www.immutep.com/technology/lag-3-technology.html)
其他临床LAG-3靶点药物
根据已有的临床药物研究来看,LAG-3药物联合其他免疫检查点抑制剂治疗是研究的主流,并且显示出了良好的治疗效果。
参考文献:
[1]Fibrinogen-like Protein 1 Is a Major Immune Inhibitory Ligand of LAG-3.[J]. Cell, 2018.
[2] Graydon Colin G,Mohideen Shifa,Fowke Keith R,LAG3's Enigmatic Mechanism of Action.[J] .Front Immunol, 2020, 11: 615317.
[3] Long Long,Zhang Xue,Chen Fuchun et al. The promising immune checkpoint LAG-3: from tumor microenvironment to cancer immunotherapy.[J] .Genes Cancer, 2018, 9: 176-189.
[4] ASCO2021
[5] Immutep: https://www.immutep.com/technology/lag-3-technology.html
[6] Jiang H , Ni H , Zhang P , et al. PD-L1/LAG-3 bispecific antibody enhances tumor-specific immunity[J].
咨询
我们尊重知识产权,如您认为本平台所载文章、图片、视频等内容侵犯您的合法权益,请您及时联系我们,我们将依据相关法律法规、平台规则予以处理。
关键字
- 348
- 点赞
- 复制链接
- 举报