研究揭示不同于经典的eIF2α磷酸化介导的蛋白重编程机制
美国杜克大学董欣年(Xinnian Dong)团队揭示了分子模式激活的免疫反应(PTI)信号通路中一个全新的蛋白翻译起始模块(Module)——PABP/R-motif介导的非帽结构依赖的胁迫相关蛋白的翻译。
美国杜克大学董欣年(Xinnian Dong)团队揭示了分子模式激活的免疫反应(PTI)信号通路中一个全新的蛋白翻译起始模块(Module)——PABP/R-motif介导的非帽结构依赖的胁迫相关蛋白的翻译。
这一发现为真核生物蛋白翻译重编程提供了不同于经典的eIF2a磷酸化通路的理论模型,对研究其他真核生物蛋白重编程具有普遍的借鉴意义。
真核生物的mRNA翻译起始(Translation initiation)是一个极其复杂的过程。在没有胁迫的条件下,绝大多数真核mRNA的翻译起始依赖于其位于5’端的m7G帽结构(Cap structure)。为了起始翻译,eIF2-GTP-Met-tRNAi三聚体与40S核糖体亚基进行组装形成43S前起始复合物(43S preinitiation complex, PIC),其中eIF2包含三个蛋白eIF2α、eIF2β和eIF2γ。
43S PIC随后被eIF4F起始复合体招募到位于mRNA 5’端的m7G帽子结构启动对mRNA从5’端到3’端的扫描,直至遇到合适的起始密码子,其中eIF4F复合体包括 m7G帽结构结合蛋白eIF4E、支架蛋白eIF4G和解旋酶eIF4A。起始密码子的识别会招募60S核糖体亚基,形成80S起始复合体开始蛋白的合成。值得注意的是,与3’端poly(A)结合的PABP(Poly(A)-binding protein)可以促进43S PIC的招募过程。
在遭遇胁迫时,真核生物通常通过eIF2α磷酸化抑制经典的m7G帽结构依赖的翻译,同时选择性地翻译胁迫必须的调节蛋白(Stress regulators),从而实现体内蛋白翻译的重编程(Reprogramming)。然而,在植物的PTI信号通路中,通过敲除GCN2完全阻断eIF2α磷酸化并没有发现其对翻译重编程的显著影响,暗示了在植物的PTI信号通路中存在全新的蛋白翻译重编程机制。
研究发现病原菌侵染可以促进DCP蛋白(Decapping protein)去除mRNA 5’端的m7G帽结构来抑制经典的帽结构依赖的蛋白翻译(Cap-dependent translation),而在5’端先导序列(Leader sequence)含有R-motif(Purine-rich element)的抗病相关mRNA,则可以利用R-motif作为m7G帽结构的代替者(Cap surrogate)——一个新式的胞内IRES(Internal ribosome entry site),结合PABP蛋白来选择性地启动自身的翻译。
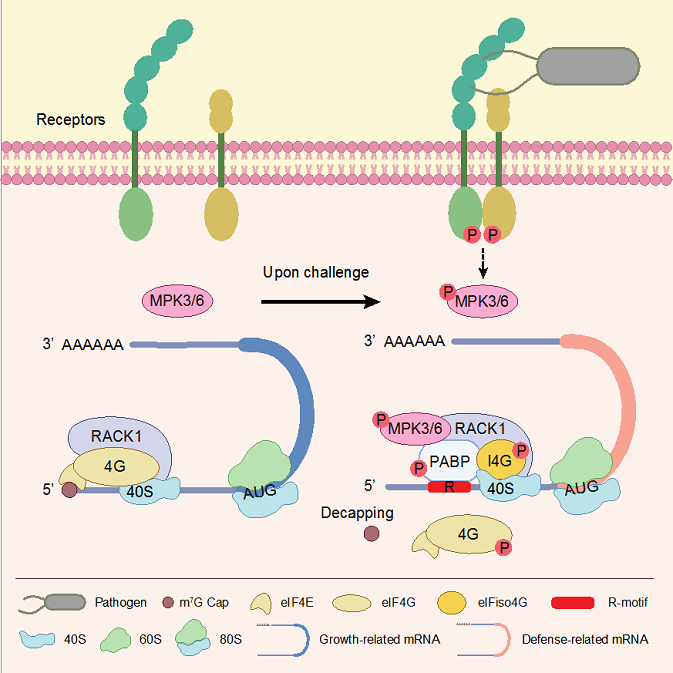
在正常生长条件下,不含有R-motif的生长相关的mRNA通过m7G帽结构依赖的方式进行翻译。当PTI信号被激活后,PABP会选择性地结合激活后的eIFiso4G(eIF4G异构体)促进含有R-motif的抗病相关mRNA的翻译。
值得注意的是,从经典的m7G帽结构依赖的蛋白翻译到R-motif介导的非帽结构依赖蛋白翻译的转变,是通过PTI信号通路中的关键激酶MPK3/6 来实现的。当PTI信号被接受后,MPK3/6会被激活,诱导mRNA去除5’端的帽子结构,并磷酸化eIF4G来抑制生长相关mRNA的翻译;同时磷酸化PABP增强其与R-motif之间的结合,激活eIFiso4G蛋白,促进含有R-motif的抗病相关mRNA的翻译。
研究揭示了不同于经典的eIF2α磷酸化介导的蛋白重编程机制,同时因为R-motif同样广泛存在于果蝇、小鼠和人体的胁迫相关mRNA的5’端前导序列中,研究发现的蛋白翻译起始调控机制可能同样广泛存在于其他真核生物体中。
咨询
- 151
- 点赞
- 复制链接
- 举报