一起学习吧 | 蛋白质纯度、浓度常用实验方法
蛋白质纯度、浓度实验方法是生物化学研究中常用的分析技术,它们可以帮助我们评估蛋白质样品的质量、稳定性、活性和功能。这些方法对于蛋白质的表达、纯化、鉴定、结构分析、功能研究等都有重要的意义。
蛋白质纯度是指蛋白质样品中目标蛋白质的含量或比例,它反映了蛋白质样品中是否存在其他杂质或污染物,如核酸、多糖、脂质、无关蛋白质等。
蛋白质纯度的测定可以帮助我们评价蛋白质的分离效果,选择合适的纯化步骤和条件,优化纯化方案,提高纯化效率和产量。
同时,蛋白质纯度也影响了蛋白质的活性和功能,高纯度的蛋白质更容易保持天然构象和生物活性,更适合进行结构分析和功能研究。
本文将简要介绍常用的蛋白质纯度、浓度检测试验方法。
“经典技术,长久不衰”
电泳是一种利用均匀电场的作用,使混合物中的不同大小和/或电荷的颗粒在流体中运动并分离的实验技术。
聚丙烯酰胺凝胶电泳(PAGE):使用凝胶作为固相,将含有目标蛋白质的溶液加载到凝胶中的小孔上,然后将凝胶两端连接到带有不同极性的电源上,使电流通过凝胶。根据蛋白质的大小和电荷,它们会以不同的速度和方向在凝胶中迁移,形成不同的条带。
聚丙烯酰胺凝胶电泳(PAGE)具有多种形式,根据不同的条件和目的,可以分为以下几种:
➤非还原凝胶电泳:这种形式的PAGE不使用任何变性剂或还原剂,保持了蛋白质的原生态结构和活性。它主要受蛋白质的电荷和形状的影响,而不是大小。它适用于分析蛋白质的复合物、结合能力、等电点等。
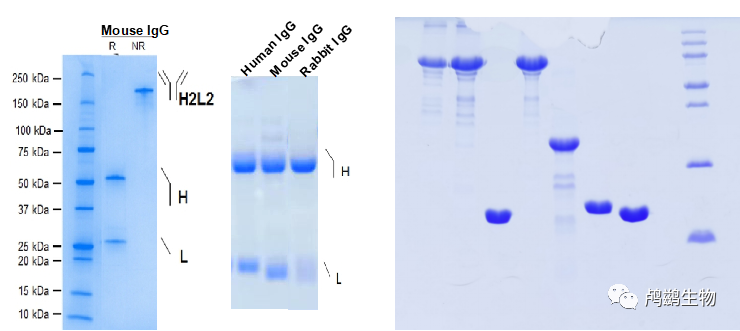
➤SDS-PAGE:这种形式的PAGE使用十二烷基硫酸钠(SDS)作为变性剂,使蛋白质呈线性化,并赋予负电荷。它还可以使用β-巯基乙醇或二硫苏糖醇(DTT)作为还原剂,打开蛋白质的二硫键。这样,蛋白质就只根据大小进行分离,而不受电荷和形状的影响。它适用于测定蛋白质的分子量、纯度、组成等。

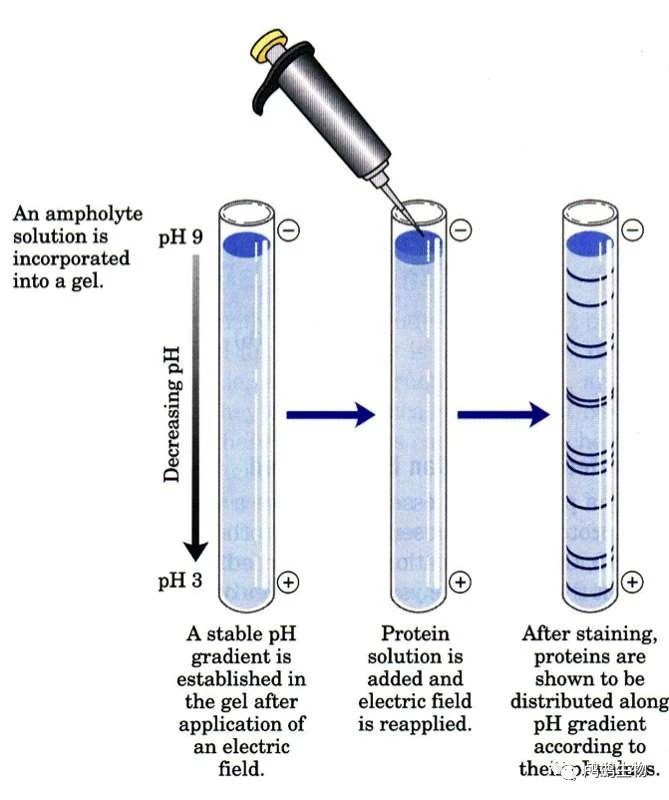
➤IEF(等电聚焦)电泳:这种形式的PAGE使用一种特殊的凝胶,称为等电聚焦凝胶,它具有pH梯度,从低到高。当蛋白质在电场中迁移时,它们会在与其等电点相对应的pH处停止,因为此时它们没有净电荷。这样,蛋白质就根据其等电点进行分离,而不是大小或形状。它适用于分析蛋白质的异构体、变异体、修饰等。
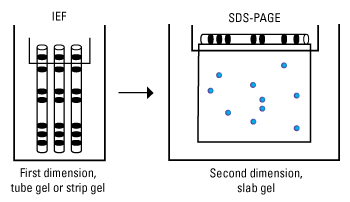
➤二维凝胶电泳:这种形式的PAGE结合了两种不同类型的PAGE,通常是IEF和SDS-PAGE,以实现更高维度和分辨率的分离。首先,在第一维中,将蛋白质按照等电点进行分离;然后,在第二维中,将第一维中得到的条带按照大小进行分离。这样,蛋白质就根据两个参数进行分离,并在凝胶上形成点阵图案。它适用于分析复杂的蛋白质混合物、表达谱、差异表达等。
电泳后需要对蛋白质进行可视化,以便于识别和定量。可视化方法有多种,例如:
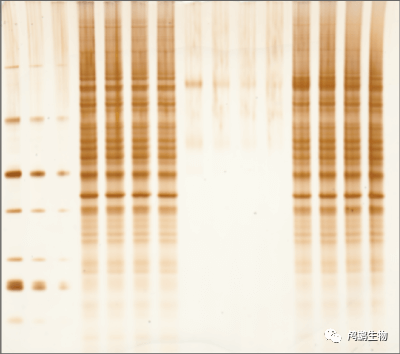
➤银染剂染色:利用银染剂能够与蛋白质反应并产生棕色沉淀的特性,对蛋白质进行染色和检测。
➤考马斯亮蓝染色:利用考马斯亮蓝能够与蛋白质结合并产生蓝色复合物的特性,对蛋白质进行染色和检测。
“生物人必备技能”
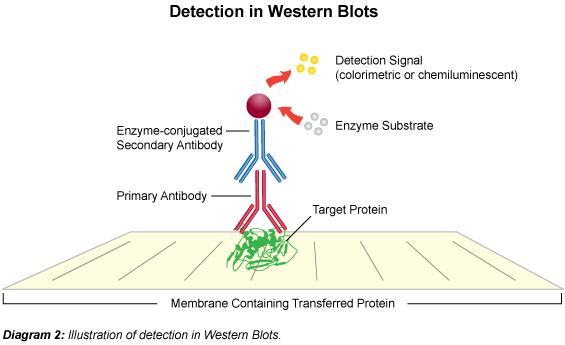
利用特异性抗体与目标蛋白质结合并产生信号的特性,对蛋白质进行转印和检测。是一种用于检测复杂蛋白质混合物中特定蛋白质的技术。
它包括以下几个步骤:
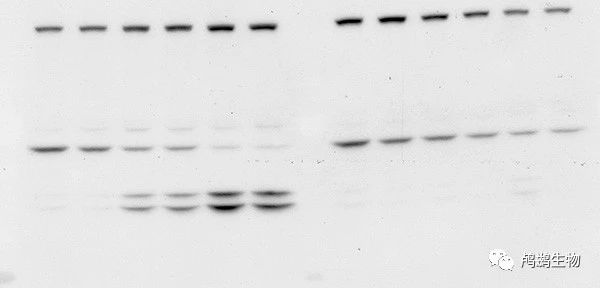
➤分离:使用凝胶电泳(如 SDS-PAGE)将蛋白质按照大小或电荷分离。
➤转移:将分离的蛋白质从凝胶转移到能够结合蛋白质的膜(如硝化纤维素)上。
➤封闭:用一种非特异性的蛋白质(如牛血清白蛋白)覆盖膜,以阻止后续步骤中的抗体与膜的非特异性结合。
➤检测:使用一对抗体来识别和可视化目标蛋白质。第一个抗体(一抗)是能够特异性识别目标蛋白质的抗原的。第二个抗体(二抗)是能够识别一抗的,并且带有一个标记,如生物素、荧光或酶。标记可以通过染色、发光或变色来显示目标蛋白质的位置和数量。
“甩板、拍板”的酸爽后劲十足
是一种常见的实验室技术,设计用于检测和定量分析物(通常是抗体或抗原)。
ELISA 有多种形式!最常用的是“三明治”形式(夹心Elisa),原理是利用两种抗体来夹住目标抗原,形成一个类似三明治的复合物,然后通过酶标记的二抗来产生信号。这种方法的优点是可以提高检测的特异性和灵敏度,缺点是操作步骤较多,且需要两种高度特异性的抗体。
单克隆抗体具有高度的特异性和一致性,多克隆抗体具有高度的亲和力和灵敏度。在ELISA实验中,单克隆或多克隆抗体均可用作夹心ELISA系统中的捕获和检测抗体,采用单克隆抗体和多克隆抗体的组合配对方式进行实验设计,可以平衡特异性和亲和力。单克隆抗体识别单个表位,可精细检测和定量抗原的微小差异。通常使用多克隆抗体作为捕获抗体,以沉降尽可能多的抗原。
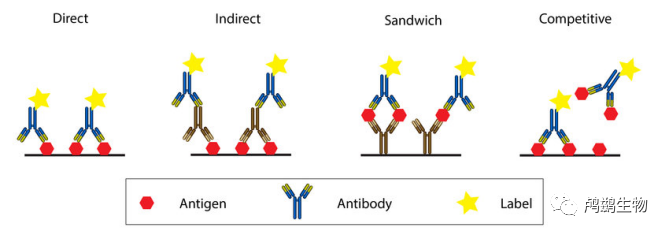
除了“三明治”形式外,ELISA 还有其他几种形式,例如:
• 直接 ELISA:这种方法只需要一种直接偶联酶的抗体来检测目标抗原。它的优点是操作步骤简单,缺点是需要制备不同的偶联抗体,并且可能出现较高的背景信号。
• 间接 ELISA:这种方法类似于直接 ELISA,但是使用两种抗体,一种结合目标抗原,另一种偶联酶并结合第一抗体。它的优点是可以使用同一种偶联二抗来检测不同的目标,并且可以放大信号,缺点是操作步骤较多,并且可能增加非特异性结合。
• 竞争性/抑制性 ELISA:这种方法利用已知浓度的标准品和未知浓度的样品与同一种偶联酶的抗体竞争结合。它的优点是可以检测小分子或相似结构的抗原,并且不受干扰物的影响,缺点是需要制备标准品,并且信号与浓度呈负相关。

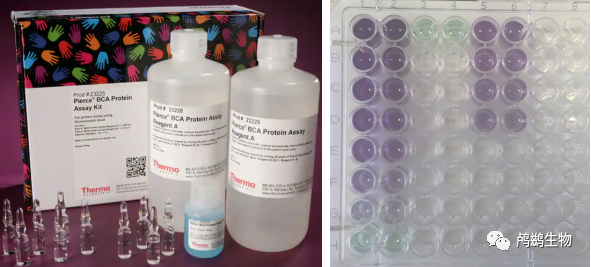
那是一抹深浅不一的紫色
BCA 测定是一种常用的蛋白质定量方法,利用缩二脲反应,其中蛋白质主链螯合 Cu2+ 离子并将其还原为 Cu1+ 离子。然后,Cu1+ 离子与二辛可宁酸 (BCA) 反应,形成在 562 nm 处吸收的紫色产物。
它的优点是具有较高的灵敏度、稳定性和可重复性,适用于大多数生物样品,如血清、尿液、细胞裂解液等。
它的缺点是受到一些干扰物的影响,如脂肪酸、糖类、胆汁酸等,并且对不同的蛋白质响应不同。
分分钟内出“答案”,记得考虑上蛋白质的消光系数
利用蛋白质分子中的芳香族氨基酸(如色氨酸、酪氨酸)在 280 nm 处具有较强的紫外光吸收的性质,来测定蛋白质浓度的方法,苯丙氨酸和二硫键,在这个波长也有轻微的吸光度。
它的优点是简单、快速、无需添加任何试剂,需要的样品量很小。
缺点是受到其他吸收紫外光的物质(如核酸、表面活性剂、缓冲液等)的干扰。

联系我们
鸬鹚生物技术有限公司
成都研发中心:双流区永安镇天府国际生物城凤凰路269号
贵州生产基地:贵州黔南州龙里县冠山街道高新技术产业园区
咨询
- 228
- 点赞
- 复制链接
- 举报