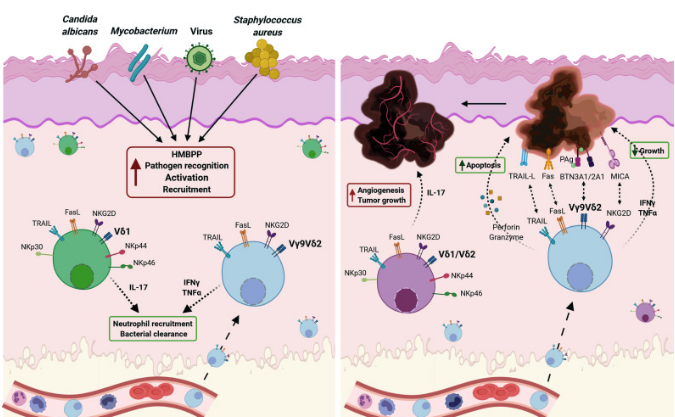
新冠肺炎中的NK细胞功能障碍(dysfunction)及策略
1. 自然杀伤细胞在免疫调节中的作用
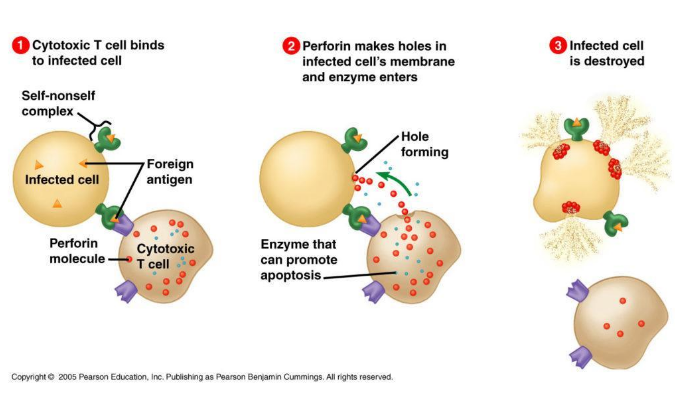
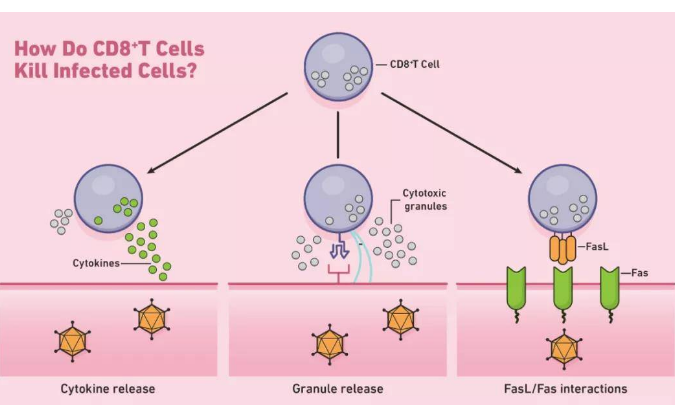
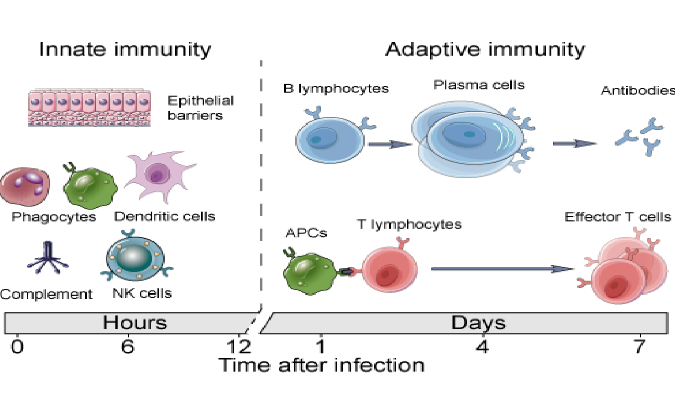
自然杀伤(NK)细胞是先天免疫系统的一部分,它们是预防急性感染和癌症的第一道防线(固有免疫),同时还调节适应性免疫反应。NK细胞功能受到激活和抑制性受体平衡的严格调控。NK细胞活化导致细胞毒性颗粒和炎性细胞因子的产生,杀死靶细胞。健康细胞表达主要的组织相容性复合物I类(MHC I)分子,这些分子将这些细胞标记为“自我”,MHC I充当NK细胞上抑制性受体的配体,并通过防止NK细胞对这些细胞的杀伤来促进“自我耐受性”。MHC I-特异性抑制受体包括杀伤细胞免疫球蛋白样受体(killer cell immunoglobulin-like receptors KIRs)(KLRG1和TIGIT)和凝集素样CD94-NKG2A异源二聚体。与感染或癌症生长相关的细胞应激、KIR参与受损和MHC I表达下调会降低抑制性信号传导阈值,从而导致NK细胞活性受体上调。NK细胞表达多种激活受体,这些受体通常在机体受到感染或其他应激情况下,诱导触发NK细胞反应的信号通路(NKG2D,CD244,NKp30,NKp46)。通过共激活,这些受体克服了NK调节平衡,从而获得了有效的反应。活化的NK细胞通过多种机制诱导杀伤;(1)NK细胞活化可以通过穿孔素和颗粒酶B的细胞毒性导致靶细胞的直接裂解,(2)通过产生炎症细胞因子间接消除靶细胞,例如干扰素-γ(IFN-γ)和肿瘤坏死因子α(TNF-α),(3)NK细胞表达CD16,其是一种FcR,可以导致NK细胞产生抗体依赖性细胞毒性作用(ADCC)和(4)通过与辅助细胞的相互作用,例如单核细胞,诱导IFNγ产生并增强细胞毒性。
NK细胞可分为CD56dim和 CD56bright亚型 (图 1).CD56dimCD16+ NK细胞在血液中含量丰富,具有细胞毒性,表达穿孔素并产生IFN-γ,CD56+brightCD16-细胞存在于淋巴组织中,这些细胞缺乏穿孔素活性,但在IL-12,IL-15和IL-18的刺激下会产生细胞因子如IFN-γ,增强NK细胞杀伤效应。
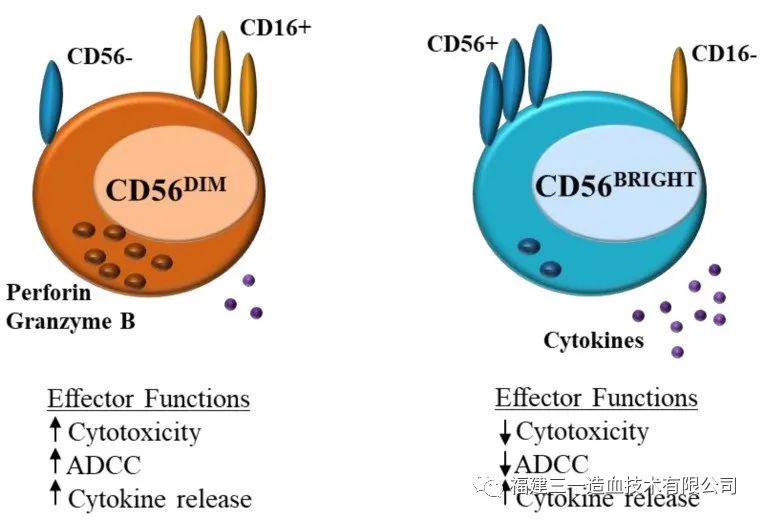
图 1 CD56dim和CD56brightNK细胞的功能差异。
除了它们在病原体清除中的关键作用外,NK细胞的一个同样重要的作用是它们限制免疫反应的潜力,特别是T细胞。这是间接通过调节抗原呈递细胞(例如树突状细胞(DC))和直接通过与T细胞本身的相互作用来实现的。在急性感染期间,NK细胞可以通过IFNγ的分泌促进幼稚的CD4 + T细胞分化为Th1 T细胞,从而导致对病原体控制增加,它们还可以通过分泌IL-10减少T细胞启动。此外,NK细胞也通过细胞毒性杀死活化的T细胞来调节适应性免疫反应。活化的T细胞通常表达更高水平的激活配体(NKG2D)和更低的抑制性配体(MHC I),这可以导致它们的识别和消除。由此导致的T滤泡辅助细胞(Tfh)的减少进一步阻碍了B细胞反应的发展,而Tfh细胞负责协助/驱动B细胞分化成产生抗体的记忆B细胞和浆细胞。
2. COVID-19的免疫学特征
SARS-CoV-2是2019年冠状病毒病(COVID-19)的病原体。这场持续存在的大流行在全球范围已感染数亿人口,而且造成了数百万人口的死亡。SARS-CoV-2 感染在大多数情况下的特征是发热、疲倦和干咳等轻度症状。在极少数情况下,可以导致严重的并发症,如细胞因子释放综合征(CRS),噬血细胞淋巴组织细胞增多症(HLH)和急性呼吸窘迫综合征(ARDS),这些严重并发症在老年人中更常见,尤其是心血管疾病患者。
与SARS一样,COVID-19的免疫病理学产生是基于先天性和细胞介导的免疫反应的失调。SARS-CoV-2也被证明利用ACE2作为细胞进入受体,已有研究表明ACE2在肺部和心血管疾病中的活性均增加。多项研究发现,感染SARS-CoV-2的患者NK和CD8+T细胞数量显著减少,这些细胞表现出功能性衰竭表型,NK抑制性标志物NKG2A和T细胞衰竭标志物PD-1和Tim-3的表达增加。在NK细胞中,抑制性标志物NKG2A的表达导致IFNγ,IL-2和TNFα的表达降低以及颗粒酶B水平降低。与Tim-3在T细胞中的衰老作用相反,有人认为它是具有正常功能的NK细胞的标志物,可以导致IFNγ表达增加。然而,也有研究表明,Tim-3与NK细胞细胞毒性的受限有关。Wilk等人的一项研究发现,COVID-19患者的NK细胞上还有另外3种耗竭标志物(LAG3、PDCD1和HAVCR2),表明SARS-CoV-2感染很可能诱发了衰竭的NK细胞表型。未来的研究将充分阐明耗竭标志物在COVID-19中NK功能中的作用。此外,一些研究中还观察到COVID-19患者有较高的中性粒细胞与淋巴细胞比率,表明全身炎症和感染,基因表达分析表明,在COVID-19中,NK功能和成熟度特有的各种基因均下调表达,特别是细胞毒性CD56dimNK细胞FCGR3A和FGFBP2的表达。综合这些发现都表明,SARS-CoV-2感染中存在更具炎症性的NK细胞表型。
COVID-19患者表现出高水平的炎性细胞因子和趋化因子(IL-1a/β、IP-10、MCP-1),重症病例显示TNFα、IL-1、IL-6、IL-18、IL-8、IL-10、MCP-1和MIP-1A升高,导致严重肺组织损伤,除炎症作用外,IL-1还与COVID-19患者中血栓素-A2的表达有关,导致血小板活化和聚集增加,从而介导血栓形成。NK细胞很可能在这种细胞因子诱导的损伤中起重要作用。首先,趋化因子MCP-1和IP-10招募NK细胞到发炎的组织,特别是肺,然而这些NK细胞的效应功能钝化并偏向炎症表型。有研究表明,NK细胞产生的IFN-γ和TNF-α可能通过NF-κB依赖性上调ICAM-1在靶细胞中的表达从而清除靶细胞。的NK细胞数量的减少以及通过NKG2A表达诱导的IFN-γ和TNF-α水平的降低,可能导致SARS-CoV-2中NK细胞裂解靶细胞功能降低。最后,IL-6和IL-10是SARS-CoV-2感染的一个突出特征,两者都具有降低NK细胞毒性的能力(图2)。IL-6已被证明可直接降低穿孔素和颗粒酶B的表达,事实上,Mazzoni等人发现,血清IL-6水平与NK细胞表达颗粒酶A的频率呈负相关,特别是在重症患者中。而IL-10已被证明通过降低IFN-γ和IL-2表达而与NK细胞细胞毒性呈负相关。在病毒感染中,NK细胞毒性能力的下降导致抗原刺激的积累,使炎症永久化,并引发组织损伤。在重症COVID-19病例中,辅助性T细胞、调节性T细胞和记忆性T细胞均减少,但Th1和Th2细胞因子水平仍然较高。综合这些因素表明,NK细胞毒性和免疫调节减弱可导致SARS-CoV-2感染中的关键炎症表型。
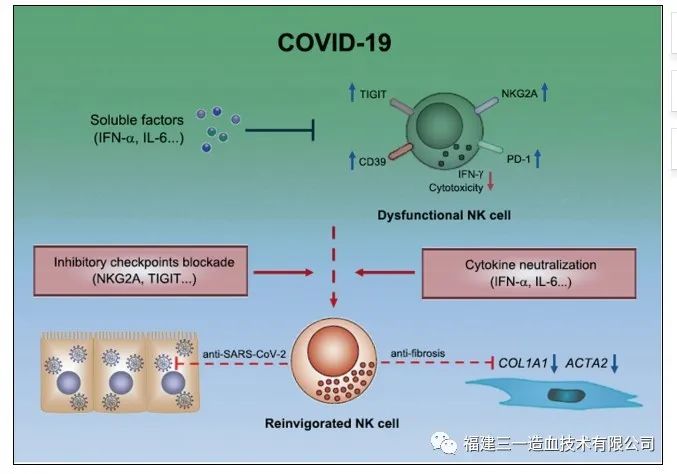
图2. COVID-19中NK细胞功能异常(Bi. 2022)
关于NK细胞激活受体在SARS-CoV-2感染中的作用知之甚少。在其他呼吸道病毒(如RSV、流感和腺病毒)中,已经描述了各种抑制机制。NKG2D通过数个配体具有广泛的活化能力,NKG2D表达和功能的降低允许病毒逃逸,从而导致促炎细胞因子表达增加以及加重肺部炎症表现。在RSV中,可溶性MICA的增加抑制NKG2D活性,而在人巨细胞病毒中,这是通过早期表达I型IFN和IL-12来实现的。流感病毒神经酰胺酶蛋白允许流感病毒逃避NKp46和NKp44识别,从而显著减少对感染细胞的杀伤。NKp46已被证明是呼吸道病毒感染患者鼻腔灌洗中最主要的细胞毒性受体。有研究观察到NKp46剪接异构体的变化,异构体之间的功能差异很明显,NKp46结构域1阴性亚型被证明在功能上更活跃。此外,还观察到细胞因子调节NKp46剪接变体表达谱。亦有证据表明,NKG2C的低表达可能导致更严重的SARS-CoV-2结果,上述结果是初步的,仍需要更多的研究来了解SARS-CoV-2对NK细胞激活受体的影响。
许多临床试验正在研究直接影响NK效应细胞功能的治疗策略。免疫抑制药物Tocilizumab和Anakinra分别阻断IL-6和IL-1,导致穿孔素、颗粒酶A/B和IFNγ的表达增加。托西利昔单抗已被证明可恢复4/5 COVID-19 ICU患者的NK细胞毒性活性。CYNK-001是从胎盘造血干细胞开发的冷冻保存的同种异体NK细胞疗法,这些细胞表达NK激活受体NK2D,DNAM-1和细胞毒性受体NKp30,NKp44和NKp46,它们还表达穿孔素和颗粒酶B。另一种NK细胞疗法是IL-15超级激动剂和粒细胞巨噬细胞集落刺激因子(GM-CSF),中和来自脐带血的分泌scFv的NKG2D-ACE2 CAR-NK。该治疗可阻断ACE2呈递细胞的SARS-CoV-2感染,同时上调NK细胞的细胞毒性。羟氯喹(HCQ)和静脉注射免疫球蛋白(IVIG)等治疗可以通过减少T细胞活化和引入功能性免疫细胞间接改善NK细胞功能。一些试验还在研究在SARS-CoV-2感染的早期治疗中使用氧气治疗,因为先前的研究表明,该治疗可有效减少炎症,减少IL-12和TNF-α,并增加IL10。许多试验正在调查用于保护幼儿免受结核病(结核分枝杆菌)侵害的卡介苗(BCG)可能通过训练有素的免疫提供针对SARS-CoV-2的异源保护的可能性。BCG疫苗接种可能导致单核细胞和NK细胞群的表观遗传改变,从而增强对后续感染的免疫应答,特别是通过增加IL-1β、TNF和IL-6的表达。
此外,类黄酮槲皮素和木犀草素已被证明可降低肥大细胞中IL-6的表达,可能是皮质类固醇治疗的更安全的替代药物。而抗炎细胞因子的作用亦不容忽视,尽管尚未进行人体试验,但IL-37已被证明可以抑制类风湿性关节炎的全身炎症和流感小鼠模型。IL-37和IL-38均被推荐为潜在的COVID-19治疗方法。在COVID-19中改善NK细胞功能的目标中,最后一个考虑因素是锻炼。缺乏身体活动已被证明会降低NK细胞活性和IFN-γ表达。遏制SARS-CoV-2传播的隔离和封锁策略无意中导致许多人遵循更不活跃的生活方式。加强身体活动的重要性,特别是在高危人群中,可能对COVID-19结果有益。
此外,除细胞因子外,越来越多的证据表明,NK细胞上的抑制性检查点受体可能导致COVID-19相关NK细胞的功能失调状态。例如,Demaria等人在外周血和支气管肺泡灌洗液中检测到较高水平的NK-19相关NK细胞中的NKG2A、PD-1和CD39。阻断NKG2A与其配体与抗NKG2A单克隆抗体的相互作用增强了COVID-19患者NK细胞的细胞毒性活性。另一方面,Krämer等人在一些COVID-19患者中检测到NK细胞上的TIGIT表达增加。TIGIT NK细胞比COVID-19患者的TIGIT NK细胞产生更多的IFN-γ。这些研究表明,COVID-19患者中NK细胞的活性受到抑制性检查点受体的抑制。
3. 使用离体扩增NK细胞纠正Covid-19患者NK细胞障碍的可行性
COVID-19患者中的一部分可能在感染后的后期阶段发展为严重的肺炎和纤维化肺损伤。有效的抗病毒免疫和预防纤维化进展对于控制COVID-19至关重要。自然杀伤(NK)细胞的靶向策略已经在肿瘤免疫治疗中显示了治疗益处,Krämer等人最近提供了NK细胞显示出抗SARS-CoV-2活性的证据。他们的研究表明,来自健康个体的纯化外周NK细胞降低了共培养SARS-CoV-2感染细胞中的病毒蛋白水平。NK细胞产生的效应细胞因子IFN-γ和TNF-α对这一过程至关重要。除抗病毒活性外,NK细胞还具有限制组织纤维化的功能。Krämer等人研究表明,来自对照个体的IL-2激活的NK细胞降低了人肺成纤维细胞中促纤维化标志物基因COL1A1和ACTA2的表达,这表明NK细胞通常在肺中可能具有抗纤维化活性。根据这些研究数据表明,NK细胞可能通过抑制病毒和抑制纤维化进展来改善对COVID-19的控制。
然而,与先前对COVID-19相关NK细胞的研究一致,Krämer等人表明,来自COVID-19患者的NK细胞表现出类似于肿瘤相关NK细胞的功能失调状态,这可能会损害其抗SARS-CoV-2活性和潜在的抗纤维化活性。首先,COVID-19患者中循环NK细胞的绝对数量减少,特别是在患有严重疾病的个体中。NK细胞数量的这种减少与炎症强度相关,并且可能是由病毒诱导的细胞凋亡引起的,因为SARS-CoV-2核衣壳蛋白增加了NK细胞中活性半胱天冬酶-3和CD95的表达水平。COVID-19相关NK细胞的数量和“质量”都受到损害。单细胞转录组学分析表明NK细胞组成改变,其中,在重症患者中炎性CD56dim亚群(选定的标记基因:IFI6、ISG15、IFI44L、XAF1、MX1、PRF1、GZMB和 FCGR3A)和”增殖 CD56dim“亚群(选定的标记基因:MKI67、LGALS1、STMN1、TUBA1B 和 HMGB2)表达增多。更重要的是,COVID-19相关NK细胞降低SARS-CoV-2感染细胞中病毒蛋白水平的能力显着低于对照组正常NK细胞,这可能是由于COVID-19相关NK细胞IFN-γ和TNF-α的产生减少所致。此外,来自COVID-19重症患者的NK细胞表现出与肺纤维化患者的肺NK细胞相似的基因表达特征(AREG,DUSP2,ZFP36L2和TSC22D3的上调),伴随着抑制促纤维化标志物基因COL1A1和ACTA2表达的能力受损。综上所述,COVID-19相关的NK细胞在抗SARS-CoV-2活性和抗纤维化活性方面都显示出功能受损害。
Bao et al实施的一项研究回顾性地招募了168名COVID-19患者,按照指定的方法进行随访和分析。非重度组和重度组在白细胞、中性粒细胞、淋巴细胞、嗜碱性粒细胞和血小板计数以及CRP和血清细胞因子IL-6等感染相关参数方面表现出显著差异。重症组的CRP和IL-6水平高于非重度组。对于入院时的淋巴细胞亚群测定显示重症组的淋巴细胞计数明显低于非重度组。入院后,每周至少进行两次病毒RNA检测以及特异性IgM和IgG检测。外周血中总T细胞,CD4 + T细胞,CD8 + T细胞和NK细胞的较高计数与获得第一次阴性病毒RNA检测和第一次阳性IgM / IgG抗体检测所需的时间较短存在显着相关性:重症组需要更长的时间才能达到第一次IgM / IgG测试阳性(IgM或IgG超过10 IU / mL)。此外,有研究表明炎症性单核细胞在COVID-19患者中分泌IL-6和GM-CSF,导致IL-6等细胞因子升高。IL-6介导的JAK / STAT信号传导,可引发细胞因子释放风暴(CRS)并与较差的预后相关。根据我们的数据,较高的CRP和IL-6与实现首次病毒RNA阴性和IgM / IgG阳性检测所需的时间较长有显着相关性。B细胞的数量仅与达到首次阳性IgM / IgG测试的时间相关。NK细胞的计数也与更高水平的IgG抗体相关(p = 0.025)。淋巴细胞减少症(<1 × 109/L)组的病毒转阴存活率(log-rank p = 0.022)和病毒转阴持续时间(log-rank p = 0.023)比正常淋巴细胞计数组差。NK细胞淋巴细胞减少症 (<0.1 × 109/L)组的病毒转阴存活率显着较差(对数排名p<0.001)和更长的持续时间(log-rank p <0.001)(图3 )。
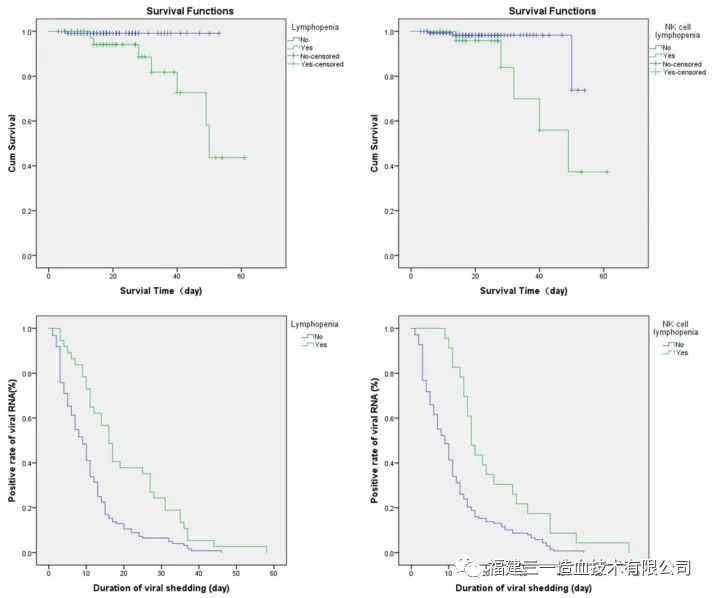
图3. 在淋巴细胞减少症亚组分析中,存活期p= 0.022,病毒脱落持续时间p = 0.023。在NK细胞减少症中,存活<0.001,病毒脱落持续时间p<0.001 (Bao et al 2022)
先天性和适应性免疫反应对于控制病毒感染至关重要。NK细胞作为先天免疫系统的一部分,在急性病毒感染期间起着重要作用。感染后IgG的强度和持续时间是SARS-CoV-2免疫的关键点。NK细胞通过杀伤细胞免疫球蛋白样受体(KIR),裂解感染细胞和释放抗原对病毒感染细胞具有直接杀伤作用。NK细胞与树突状细胞相互作用,并可能在抗原呈递和适应性免疫过程中发挥作用,起到抗SARS-CoV-2作用。NK细胞计数可能对COVID-19的IgG免疫力至关重要。考虑到COVID-19患者中尤其重症患者中NK细胞功能出现障碍,无法完全发挥清除受病毒感染细胞的作用,而NK细胞具有非MHC限制性的杀伤特点以及NK细胞不会诱发GVHD,故同种异体来源或者脐血/胎盘来源的NK细胞可能成为恢复患者自身NK功能的有效潜在手段,到目前为止,已有四项与COVID-19相关的NK细胞临床试验在Clinicaltrials.gov 注册,包括造血干细胞衍生NK细胞输注(NCT04365101),NK细胞联合标准治疗(NCT04280224),IL-15超级激动剂和GM-CSF中和scF分泌NKFV的NK-19患者NK-NK细胞疗法(NCT04324996)。同种异体来源或者脐血/胎盘来源的NK细胞更多的体内作用机制和临床效果还需要更多的研究工作支持。
4. 结论
自然杀伤细胞在维持免疫稳态方面起着核心作用,SARS-CoV-2感染已被证明会阻碍NK细胞功能发挥,从而破坏这种重要的免疫稳态。由于衰老和其他合并症如心血管等因素会导致进一步失衡,目前研究改善NK细胞功能的药物和生物制品的试验可能在我们抗击COVID-19的斗争中具有里程碑意义, 但同时也需要更多的工作来研究基于NK的免疫疗法对COVID-19患者的治疗益处。
|
货号 |
产品名称 |
作用 |
备注 |
|
CT-001 |
NK细胞高效扩增试剂盒 |
体外培养获得大量高纯度NK细胞 |
适用于脐血和外周血 |
|
FLOSEP-C-NKP |
NK细胞分选试剂盒(正) |
分选高纯度NK细胞 |
适用于脐血和外周血 |
|
FLOSEP-C-NKN |
NK细胞分选试剂盒(负) |
分选高纯度NK细胞 |
适用于脐血和外周血 |
三一造血(Stemery)版权所有,转载请注明出处 谢谢
咨询
- 381
- 点赞
- 复制链接
- 举报