高性能Aβ和Tau配对抗体→助力阿尔茨海默病诊断真正进入IVD时代
阿尔茨海默病是最为常见的神经退行性疾病,被列为威胁老人健康的“四大杀手”之一,临床症状以认知障碍为主,发病原因被认为与大脑中β淀粉样蛋白的过度产生和积累以及 tau 蛋白的过度磷酸化有关。据世卫组织估计,目前全球有超过5500万患者。估计这一数字到2030年时将上升到7800万人,到2050年时将超过1亿人。
阿尔茨海默病是进行性、不可逆的,并且无法治愈,这意味着随着时间的推移,该病会变得更严重。早期的准确诊断对于患者的早期治疗非常重要。目前,医疗机构仍依赖PET、MRI等影像学手段对阿尔茨海默病进行诊断。
近日,美国FDA近日批准上市了首款用于早期发现与阿尔茨海默病相关的淀粉样蛋白斑块的体外诊断检测产品——Fujirebio Diagnostics公司开发的Lumipulse G β淀粉样蛋白比例(1-42/1-40)检测,这标志着阿尔茨海默病诊断进入了一个新时代。该产品通过检测患者脑脊液(CSF)中β淀粉样蛋白1-42和β淀粉样蛋白1-40浓度的比例,对患者大脑中是否存在淀粉样蛋白斑块进行判断,检测结果必须与其他临床信息一起进行评估和解释。
目前,β淀粉样蛋白和Tau蛋白是阿尔茨海默病的主流IVD靶点。
★β-淀粉样蛋白1-40(Aβ1-40)和β-淀粉样蛋白1-42(Aβ1-42)
体内存在由淀粉样前体蛋白APP在不同的酶的作用下,被切割成不同长度的β-淀粉样蛋白,其中以β-淀粉样蛋白1-40(Aβ1-40)以及β-淀粉样蛋白1-42(Aβ1-42)为主。而可溶性的Aβ1-42具有神经毒性,能够减少突触数量,引发阿尔茨海默病。
★Tau蛋白和磷酸化Tau蛋白
Aβ1-42还可诱导Tau蛋白过磷酸化(p-Tau),使其在神经元内大量沉积,形成神经纤维缠结,进一步造成突触损害,最终导至阿尔茨海默病的发生。
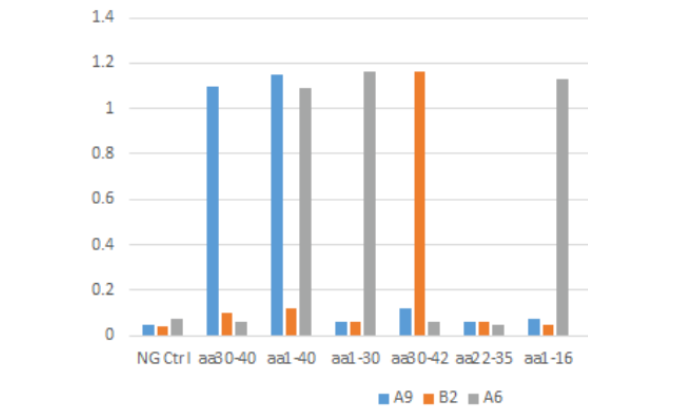
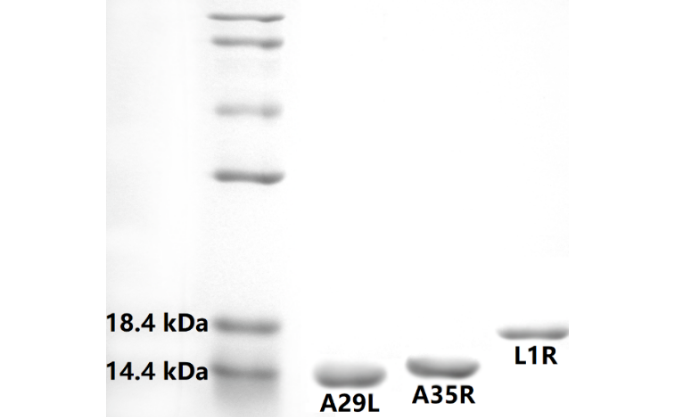
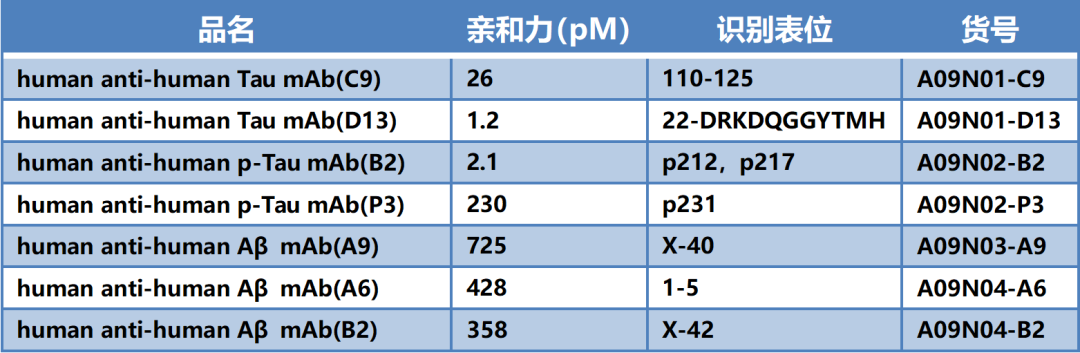
百新意生物依托抗体从头发现平台与抗原设计平台,团队目前已完成Tau、p-Tau、Aβ的抗体发现、配对验证、性能测试等工作。整套原料包括7种抗体,特异性、灵敏度、稳定性等指标或可与国内外同类产品相媲美。关于各抗体与不同抗原之间的交叉反应数据,请感兴趣者单独与技术支持联系获取。
由于脑脊液采样方式接受度较低且样本前处理尚未统一,使用外周血或尿液样本进行阿尔茨海默病检测将成为趋势,但是外周血和尿液中的蛋白标志物含量比脑脊液中低很多,这就对抗体原料的灵敏度提出了更高的要求。目前,百新意生物正在对上述抗体的检测性能进行提升,以实现从外周血、尿液中检测阿尔茨海默病标志物。
咨询
- 481
- 点赞
- 复制链接
- 举报