《人体器官捐献和移植条例》公布|数字PCR助力器官移植高质量发展,臻准在行动!
数字PCR正在逐步进入病原菌检测领域,成为一种高灵敏度、绝对定量检测手段,推动器官移植术后并发症的监测,另一方面,数字PCR步入器官移植的排斥反应检测研究中,助力无创活检技术替代组织活检方法成为可能。臻准也在不断优化和完善解决方案,相信在不远的将来,能为器官移植排斥反应和病原菌检测带来新的解决方法。
2007年颁布施行的《人体器官移植条例》,对促进器官捐献和移植事业发展发挥了重要作用。近年来,器官捐献和移植工作面临一些新情况、新形势,为了更好地保障器官捐献和移植事业健康发展,在总结实践经验的基础上,对《人体器官移植条例》进行了修订。
目前器官移植主要分为以下四类:
异种移植、自体移植、同系移植、同种移植。同种移植是最常见的器官移植,移植器官来自配型成功的捐赠者。
器官移植的主要挑战是提高移植的长期存活率和保护病人的生活质量。受体发生排斥反应以及感染并发症是移植失败最大的风险。
解决排斥反应的关键是正确的诊断与合理的治疗,而正确诊断的「金标准」就是组织病理学。通过对移植器官进行穿刺取样,确定器官存在的损伤程度及类型。但这个方法存在一些缺陷如:造成组织受损、引起并发症、易取样误差、无法实现动态监测等。
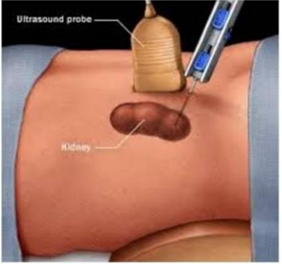
但随着一些与移植排斥反应相关的非创伤性检测指标不断出现,使得无创监测排斥反应成为新的可能。
德国的 Martina Adamek 和 Gerhard Opelz 等人发表的一篇文章,向我们介绍了一种关于实体器官移植排斥反应生物标志物检测的新方法——供者来源的游离DNA(dd cfDNA)
ddcfDNA随着移植物中的细胞坏死或凋亡而释放出来,若受者的免疫系统对移植物产生排斥反应,导致大量的细胞凋亡,则ddcfDNA的水平将居高不下。
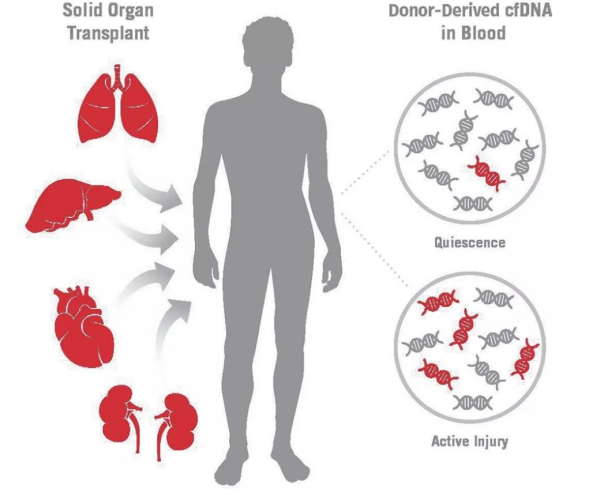
dd cfDNA常见于血液和尿液样本中,仅占受者血液和尿液中游离DNA的一小部分。目前对于dd cfDNA的检测常用以下三种方法。
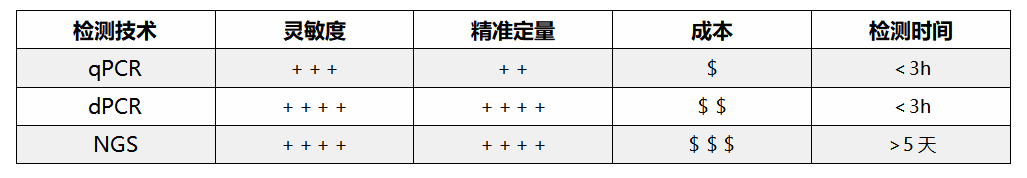
dPCR作为一种高灵敏度、能够实现绝对定量的技术,比之qPCR更适合用于含量较低的ddcfDNA的定量,其检测结果更准确。
虽然NGS法也有较高的灵敏度,但其仪器成本与技术门槛较高,且耗时较长,不适合在一般临床实验室开展。
综合来看,dPCR可能更适合应用于临床进行移植排斥的监控,这种非侵入式的监控方式能够解决上述传统方法存在的问题,提高移植的成功率及存活率。
实体器官移植后感染现状——耐药菌占比高、移植物切除风险高、病死率高,“三高”阻碍实体器官移植高质量发展。术后约有80%的受者至少出现过1次临床感染,40%的受者围术期死亡原因是感染,或其他并发症同时合并感染。
器官移植患者易发生供者来源感染和医院获得性感染,以及患者术后由于免疫抑制剂的使用,导致抵抗力下降,易发生致病菌感染。对于感染并发症的检测有利于控制器官的存活率及降低感染并发症的风险。
传统的病原体检测金标准方法是“涂片镜检法+分离培养法”,但这种方法耗时长,细菌培养一般需要1-3天,真菌培养一般需要1-3周。随着技术的发展,陆续出现了分子诊断技术、免疫学检测方法和化学法检测等病原体检测手段,目前使用最多的是分子诊断技术。第三代PCR技术-数字PCR,在病原体核酸检测方面彰显巨大优势:(1)摆脱病原微生物检测对标准品的依赖,不受抑制剂的影响;(2)数字PCR利用其灵敏度高的特点,对各种样品中的病原微生物展开检测,可以用于早期诊断和用药的低拷贝病毒的监控;(3)无需经过病原微生物培养过程,大大缩短了报告周期,及时为患者提供用药指导。

《中国实体器官移植手术部位感染管理专家共识》指出,对于有明确的感染部位/病灶但没 有病原学倾向进行血流感染检测时,建议使用数字PCR进行检测,以早期、快速和准确地对病原体进行诊断。
针对血流感染,臻准有完整的解决方案,病原菌已经覆盖大部分常见血流感染菌体和耐药靶点。
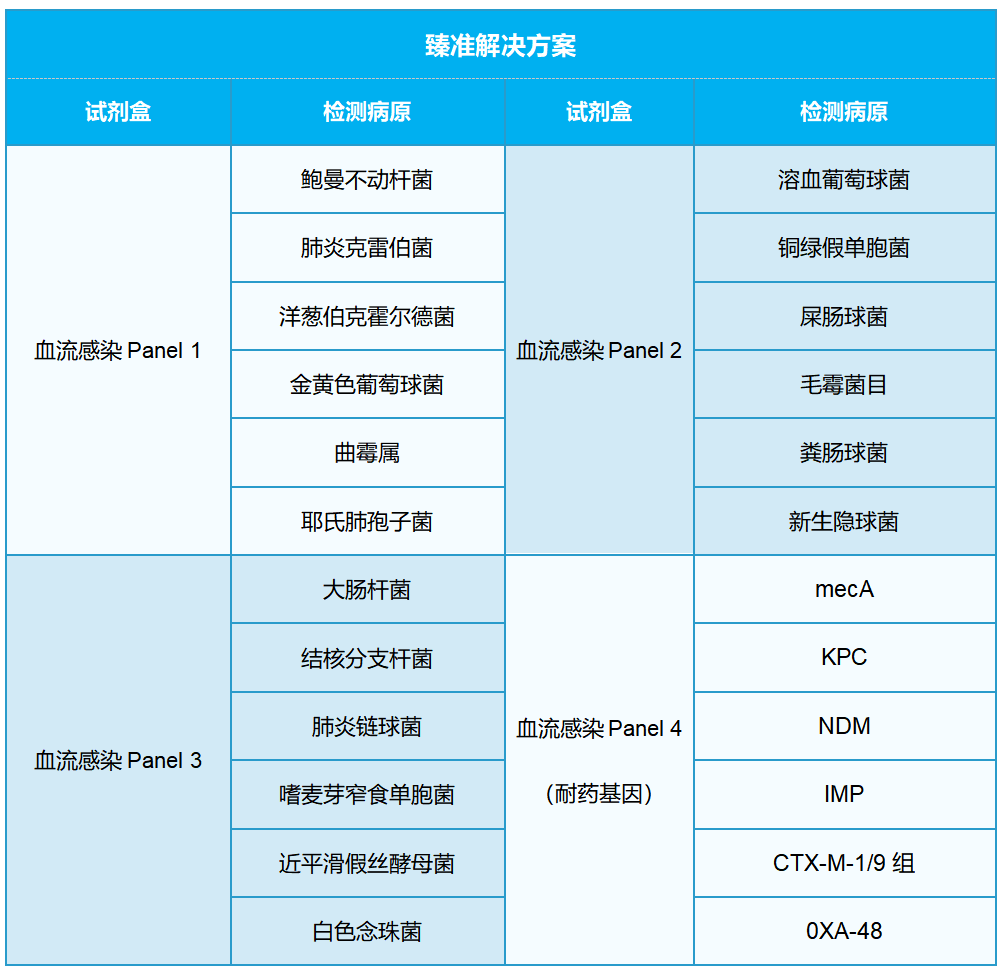
注:*该方案仅可用于辅助检测,不可直接开展临床诊断
此方案已经过大量实际样本测试,方案已步入成熟化阶段,可以广泛应用于血流感染病原菌及耐药靶点的筛查。

注:*该方案仅可用于辅助检测,不可直接开展临床诊断
数字PCR正在逐步进入病原菌检测领域,成为一种高灵敏度、绝对定量检测手段,推动器官移植术后并发症的监测,另一方面,数字PCR步入器官移植的排斥反应检测研究中,助力无创活检技术替代组织活检方法成为可能。臻准也在不断优化和完善解决方案,相信在不远的将来,能为器官移植排斥反应和病原菌检测带来新的解决方法。
咨询
- 142
- 点赞
- 复制链接
- 举报