LncRNA HOXA11-AS通过Tpl2-MEK1/2-ERK1/2通路促进胶质瘤恶性表型并降低其对ROS的敏感性
LncRNA HOXA11-AS promotes glioma malignant phenotypes and reduces its sensitivity to ROS via Tpl2-MEK1/2-ERK1/2 pathway《Cell Death and Disease》(IF=9.685)

恶性胶质瘤是最常见的原发性颅内肿瘤,癌细胞具有较高的ROS水平,并过表达抗氧化酶来保护自己免受随之而来的氧化应激的影响。
因此,提高癌细胞中的ROS水平,同时抑制其抗氧化能力,加重其氧化应激,是一种很有前途的抗癌策略。
研究团队前期的研究表明,长链非编码RNA(lncRNA)HOXA11-AS的失调在神经胶质瘤的发生发展中起着重要作用。
然而,HOXA11-AS在神经胶质瘤中的分子机制仍在很大程度上尚不清楚。
在本研究中,研究团队探讨了HOXA11-AS的异常表达和生物学功能的分子机制,以确定神经胶质瘤的新治疗靶点。
利用数据库和胶质瘤样本分析HOXA11-AS在胶质瘤中的表达,并分析了HOXA11-AS表达与胶质瘤患者预后的关系。
利用转录组学、蛋白质组学、RIP、ChIRP、荧光素酶和ChIP方法探索其在神经胶质瘤中的上下游靶点。
研究团队还研究了HOXA11-AS在调节胶质瘤细胞对活性氧(ROS)的敏感性中的作用。
研究团队发现HOXA11-AS在胶质瘤中显著上调,并与胶质瘤患者的不良预后相关。
HOXA11-AS的异位表达促进了胶质瘤细胞在体外和体内的增殖、迁移和侵袭。
在机制上,HOXA11-AS作为细胞质中let-7b-5p的分子海绵,拮抗其抑制CTHRC1表达的能力,从而激活β-catenin/c-Myc通路。
此外,c-Myc通过与其启动子区域结合形成一个自激活环,参与了HOXA11-AS的失调。
HOXA11-AS作为细胞核中的支架,也招募转录因子c-Jun到Tpl2启动子上,激活Tpl2-MEK1/2-ERK1/2通路,促进神经胶质瘤中的ROS抵抗。
重要的是,HOXA11-AS敲低可以使神经胶质瘤细胞对ROS敏感。
致癌的HOXA11-AS通过吸附let-7b-5p,上调CTHRC1作为ceRNA的表达,从而激活c-Myc来调节自身的转录。
HOXA11-AS敲低通过调节Tpl2-MEK1/2-ERK1/2轴促进神经胶质瘤细胞中的ROS敏感性,表明HOXA11-AS可能在治疗上增加ROS敏感性。
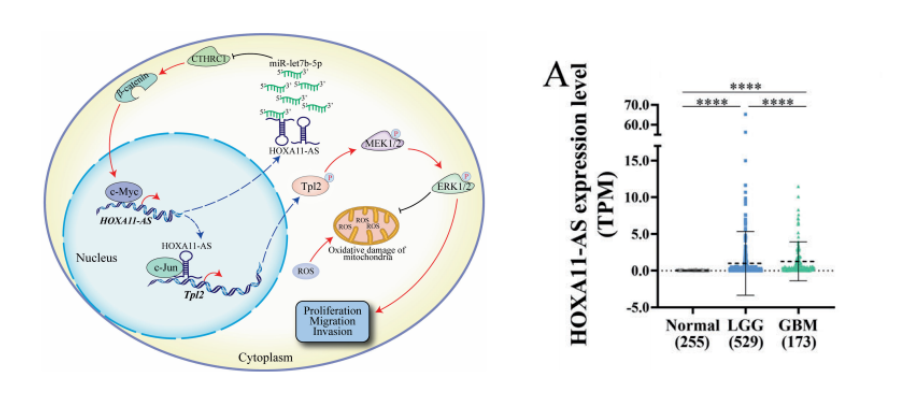
基于胶质瘤数据库的生物信息学分析,研究团队发现HOXA11-AS的高表达与胶质瘤的高级别和不良预后显著相关。
CCK-8、EdU、创面愈合和Transwell检测结果显示,HOXA11-AS可促进神经胶质瘤细胞的增殖、迁移和侵袭。
皮下异种移植实验也证实了HOXA11-AS在促进神经胶质瘤生长中的作用。
这些结果表明,HOXA11-AS高表达并促进神经胶质瘤的生长和发展,证实了其致癌功能。
HOXA11-AS是let- 7b-5p的一种竞争性内源性RNA(ceRNA)。
为了明确HOXA11-AS在胶质瘤中的分子机制,研究团队利用RIP、ChIRP、荧光素酶和ChIP方法探索其在胶质瘤中的上下游靶点。

通过ChIRP分析检测结果显示,let-7b-5p与HOXA11-AS结合,结果表明,HOXA11-AS在胶质瘤中作为let-7b-5p的ceRNA。
此外,研究团队还证实了核HOXA11-AS通过招募c-Jun到Tpl2的启动子区域来促进Tpl2的转录,从而激活Tpl2-MEK1/2-ERK1/2通路,影响胶质瘤对ROS的敏感性。
HOXA11-AS可以作为一种很有前途的预后生物标志物和新的治疗靶点来介导胶质瘤中的ROS敏感性。
作者使用伯信生物明星产品 ChIRP 试剂盒进行了上述分子互作调控机制的研究。
咨询
- 279
- 点赞
- 复制链接
- 举报





