
定点突变细胞
- RY1
- 上海睿远生物
- 上海市
- 现货
- 1次
- 0 元
- 2022-05-06 13:28:12
上海睿远生物医药科技有限公司

点突变是指基因序列中单个核苷酸碱基的改变。突变发生的位置对基因功能的影响大小不一。对非编码基因而言,大多数点突变没有什么影响;当突变位点位于基因启动子序列中时,则可能影响基因的表达;当发生在内含子剪接位点时,则可能会干扰RNA的正确剪接;当发生读码框内时,可能仅仅引起一个氨基酸的改变而改变整个蛋白的结构和功能。
从进化论的角度看,点突变既可能是有益的也可能是有害的。有益的突变使个体产生优势,并将该特性传给后代,从而使整个种群得到改善;有害突变会导致个体死亡,或通过自然选择的方式使其繁殖能力大大降低从而被淘汰。而大多数情况下我们更关注因点突变引起的疾病,如遗传性疾病镰刀性贫血症以及各种肿瘤。
通过构建点突变细胞株,可以进行单核苷酸多态性、遗传性疾病、肿瘤等的研究,也能用于靶向药、基因疗法的开发。基于大量项目的经验,睿远能够提供同源重组、单碱基编辑、先导编辑等多种技术,能够实现几乎所有位点基因突变细胞株的构建。
技术简介
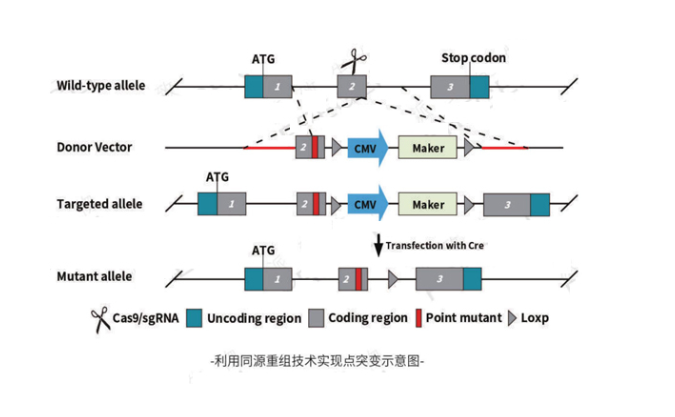
同源重组技术
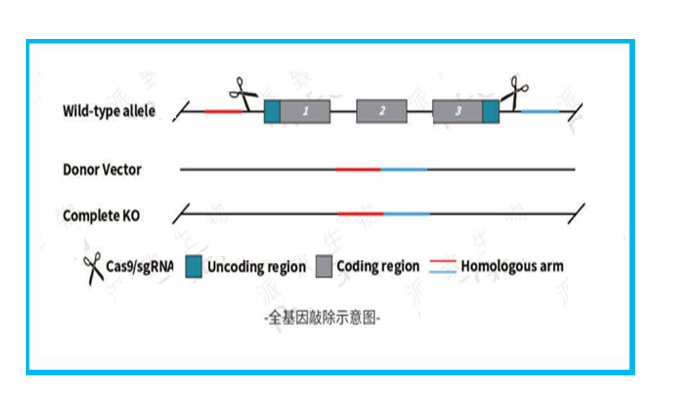
利用CRISPR/cas9技术,设计并构建cas9/sgRNA和含目的基因点突变的供体载体(Donor),将CAS9/sgRNA和Donor质粒共转染目的细胞,通过sgRNA引导Cas9核酸酶对目的基因位点进行切割,引起DNA双链断裂(Double strand breaks DSB),细胞以Donor作为模板进行同源重组修复(HDR),将目标点突变重组到基因组靶位点,从而获得目的基因点突变的细胞系。
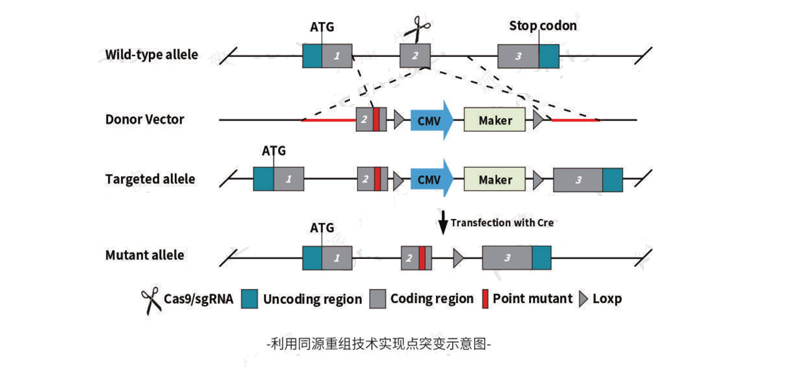
Base editing 技术
单碱基编辑技术是一种基于核酸酶失活的CAS9(dcas9)或cas9切口酶(cas9n)、胞嘧啶脱氨酶(APOBEC1)或腺嘌呤脱氨酶(TadA)以及sgRNA形成的复合体,在不断裂DNA双链的情况下,利用sgRNA将复合体靶向与sgRNA互补配对的基因组靶位点,对靶向位点进行精准编辑,实现在活性窗口内C-T、G-A、A-G,T-C的单碱基转换
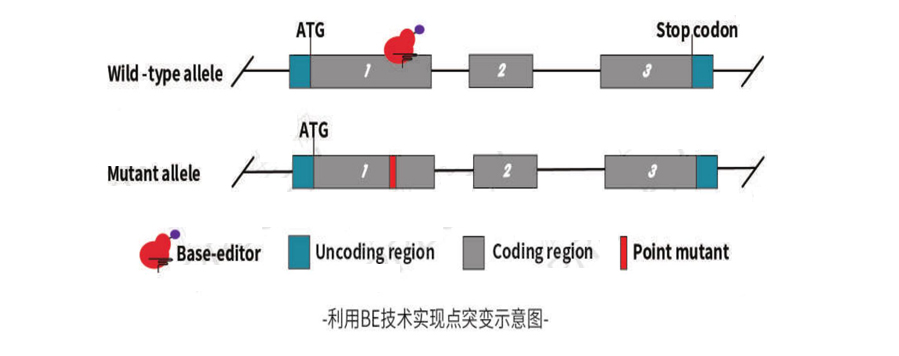
Prime editing技术
Prime editing(PE)系统是在原有的CRISPR/CAS9体系基础上进行改造开发出来的基因编辑系统,该系统包括2个元件:pegRNA(prime editing guide RNA)和nCas9(H840A)-M-MLV逆转录酶的融合蛋白。psgRNA是一段改造后的sgRNA,它在传统sgRNA的3‘末端增加了一段RNA序列。pegRNA由3个部分组成,包括Single-guide RNA(sgRNA)、引物结合位点(Prime Binding site)PBS和储存有靶向位点编辑信息的逆转录模板(RT-template)。在pegRNA的引导下,融合蛋白会靶向sgRNA互补配对的基因组靶位点,并对含PAM的靶DNA链进行切割(pegRNA的非互补链)。随后,PBS序列与被切割的目标DNA链互补配对,逆转录产物(DNA)包含我们所需要的突变位点。这段逆转录DNA会入侵并进入基因组DNA发生整合,细胞利用体内修复机制对整合DNA切口进行修复,使所需要的突变位点整合到基因组靶位点,从而获得目的基因点突变的细胞系。
应用范围
| 1 | 2 | 3 |
| 可用于单基因多态性及单碱基突变引起的疾病的研究 | 可用于靶向药、基因疗法等的开发 | 可通过引入终止密码子实现基因敲除,尤其是当目的基因存在重合基因时 |
方案选择
| 1 | 2 | 3 |
| 同源重组只能选择瞬转方案,单碱基编辑和先导编辑可选择瞬转或者慢病毒方案 | 拥有多种荧光筛选标记,结合流式分选,可提高获得阳性目的细胞的概率 | 在细胞不产生耐药的情况下,可提供多种药筛标签,满足不同实验需求 |
应用案例
细胞名称:Hep G2
基因名称:CYP3A5
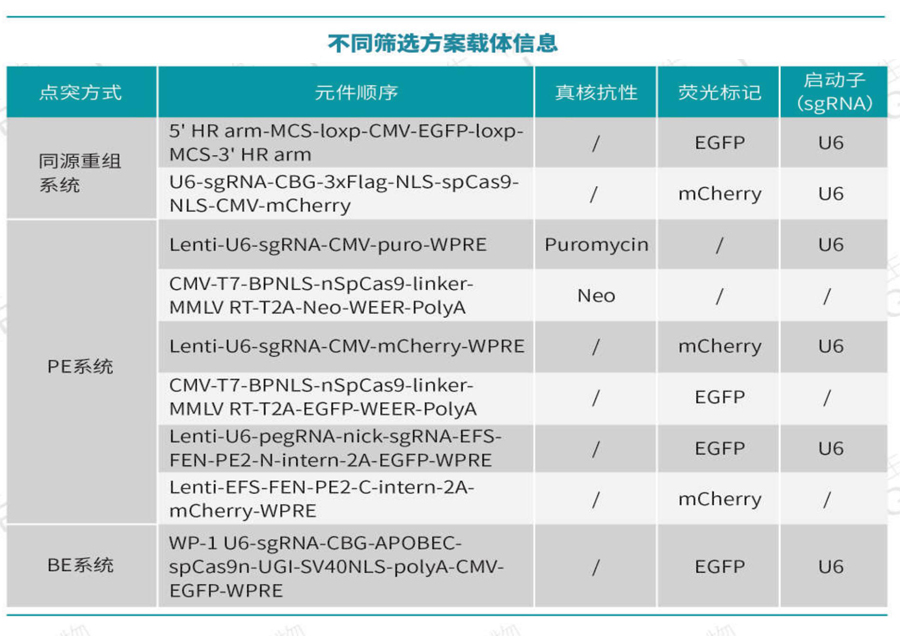
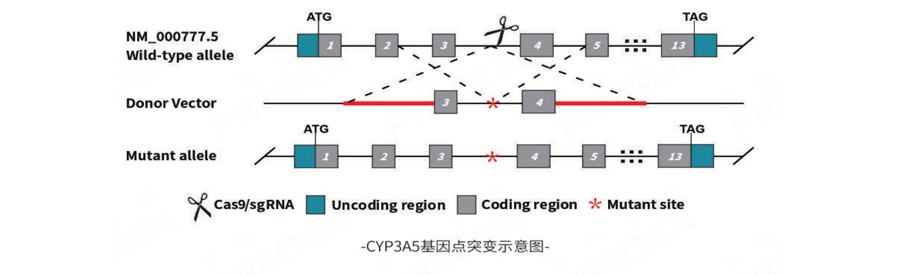
项目方案:根据CYP3A5基因突变位点序列设计sgRNA,利用CRISPR/CAS9对目的位点进行切割,引起DNA双链断裂,通过同源重组的方式将含有突变位点rs776746(A>G)的目的片段引入指定位点,通过GFP标签筛选出CYP3A5的单克隆细胞。
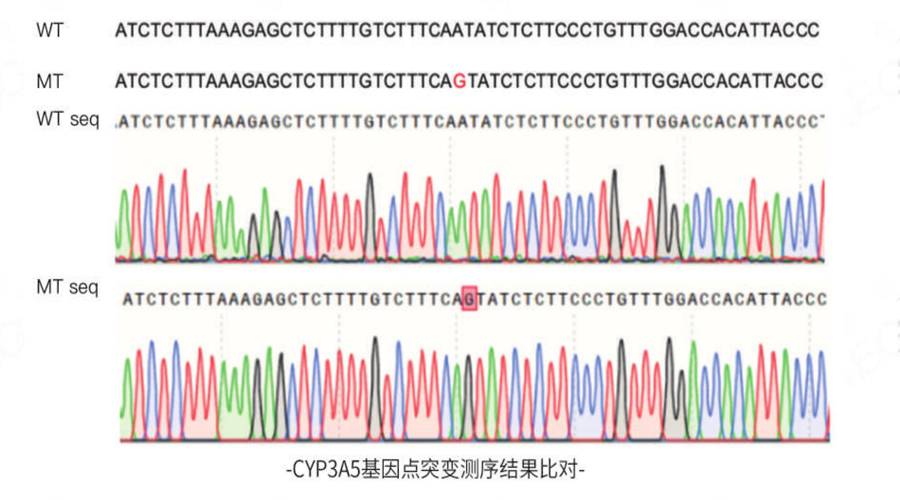
阳性细胞鉴定:通过对流式分选筛选出的单克隆细胞进行PCR及测序鉴定,CYP3A5基因rs776746位点A成功突变为G
项目流程与周期

交付标准
| 1 | 2 | 3 |
| 按指定方案构建的目的基因编辑细胞株,每个目的细胞株交付基因型正确的2个克隆,每个克隆2支冻存细胞 | 对照细胞株,瞬转方案为对应野生型细胞,慢病毒方案为CAS9稳转细胞 | 项目报告及质检报告 |