

小白说药 | 临床前成药性评价
- MDL-05
- 北京百奥思科生物医学技术有限公司
- 河北省廊坊市
- 定制协商
- 按需
- 议价
- 2023-07-28 16:58:26
北京百奥思科生物医学技术有限公司
- 关键词
- 新药研发药物研究药效测评大动物实验动物实验外包
药理学研究主要包括
临床前的药物评价主要通过对药物的药理学和药动学的研究来评价药物的安全性、有效性。其研究方法如下图所示:
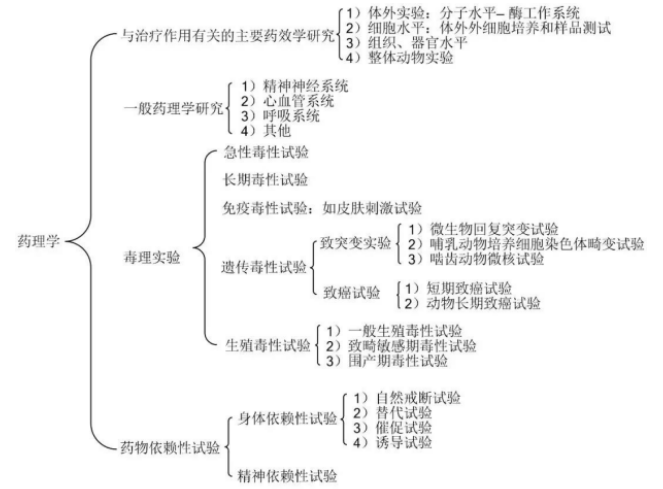
药效学实验分类:主要包括体外细胞和酶系统试验、离体器官、组织
药理学研究主要包括:
1)与治疗作用有关的药效学研究,确保受试物的有效性;
2)一般药理学研究,其目的是了解受试物主要药效作用以外的广泛药理作用,主要是研究药物对精神、神经系统、心血管系统、呼吸系统及其他系统的作用,包括安全药理学(Safety Pharmacology)和次要药效学(Secondary Pharmacodynamic)研究。
3)毒理实验,其目的是确定无害作用水平、毒性类型、靶器官、剂量-反应关系,为安全性评价或危险性评价提供重要的资料。
a. 急性毒性试验通过观察受试物一次给予动物后所引起的毒性反应和死亡情况,通过实验得到LD50(半数致死剂量)或最大给药量。LD50常与ED50(半最大效应浓度)配合计算治疗指数LD50/ED50,用以评价药物的安全性。
b. 长期毒性试验通过观察评价动物反复给予受试物后,机体产生毒性反应的特征及其毒性损害的严重程度,以及主要毒性靶器官及其损害的可逆性。试验能提供受试物的无毒性反应剂量和临床主要检测指标,为制定人用安全剂量提供参考资料。
c. 免疫毒性试验是观察药物对试验动物免疫系统产生的不良影响和影响的机理。通过试验观察动物的免疫功能是否受到抑制或产生免疫缺陷;是否降低了机体抵抗力;是否产生变态反应;以及可能引起这些反应的原因。
d. 遗传毒性试验在药物研发中处于比较的重要位置,尤其是在药物筛选阶段,在很大程度上遗传毒性试验结果将影响到药物开发的进程。通过检测基因突变、染色体畸变、染色体组畸变、DNA原始损伤来判断受试物的遗传毒性。
e. 生殖毒性试验是评价受试物对哺乳动物生殖的影响。与其他的药理学、毒理学研究资料综合比较,以推测受试物对人的生殖可能产生的毒性或危害性。
4)药物依赖性试验,药物依赖是由药物与机体相互作用造成的一种精神状态,有时也包括身体状态,表现出一种强迫性地要连续或定期使用该药的行为和其它反应,如阿片类、可卡yin、ben丙胺类等。
药动学研究内容

药动学研究是对受试物在生物体内的ADME (吸收:absorption 、分布:distribution、 代谢:metabelism、 排泄:excretion)的研究,并运用数学原理和方法阐述药物在机体内的动态规律。
吸收:药物口服后,进入消化道,在不同部位,如口腔、胃、肠吸收,进入血液。
分布:进入血液的药物进入作用部位,产生治疗作用或毒副作用。
代谢转化:药物在肝脏或胃肠道通过酶催化的一系列氧化还原反应发生生物转化。
排泄:药物或代谢物经肾(尿)或胆汁(粪)或呼吸排泄。
药动学的重要参数:
1)药物清除半衰期(half life,t1/2),是血浆药物浓度下降一半所需要的时间。其长短可反映体内药物消除速度。
2)清除率(clearance,CL),是机体清除器官在单位时间内清除药物的血浆容积,即单位时间内有多少体积的血浆中所含药物被机体清除。即体内肝脏、肾脏和其他所有消除器官清除药物的总和。
3)表观分布容积(apparent volume of distribution,Vd),是指当血浆和组织内药物分布达到平衡后,体内药物按此时的血浆药物浓度在体内分布时所需的体液容积。
4)生物利用度(bioavailability,F),即药物经血管外途径给药后吸收进入全身血液循环药物的相对量。可分为绝对生物利用度和相对生物利用度。
5)峰浓度(Cmax)和达峰时间(Tmax),指血管外给药后药物在血浆中的最高浓度值及其出现时间,分别代表药物吸收的程度和速度。
6)曲线下面积(AUC),指时量曲线和横坐标围成的区域,表示一段时间内药物在血浆中的相对累积量。

